Estenose severa de conduto de Sano tratado com implante de stent durante suporte circulatório com ECMO.
Lactante menor, sexo feminino, de 4 meses de idade com diagnóstico pré-natal de síndrome de hipoplasia do ventrículo esquerdo por atresia mitral, atresia aórtica e aorta ascendente de calibre diminuto (< 2 mm de diâmetro). A paciente foi submetida, durante o período neonatal, a uma operação de Norwood com conduto de Sano de 5 mm de diâmetro e recebeu alta 21 dias após a operação. Um mês antes de seu ingresso apresenta duas hospitalizações devido a cianose e hipoxemia, que foram interpretadas como quadros respiratórios de etiologia provavelmente viral. É transferida a nosso centro após ser hospitalizada por hipoxemia severa (Saturação de oxigênio de 60%). Ingressa conectada a ventilação mecânica invasiva com parâmetros moderadamente elevados e com hipoxemia grave. Requer ventilação mecânica invasiva com fração inspirada de oxigênio de 100% e apoio com drogas vasoativas em doses altas (epinefrina 0,2 mcg/Kg/min e norepinefrina 0,2 mcg/Kg/min) para alcançar uma saturação arterial de oxigênio sobre 60% e uma pressão parcial de oxigênio superior a 20 mmHg. Evolui em regulares condições gerais, apresentando episódios de bradicardia até a assistolia secundários à hipoxemia severa. Seu ecocardiograma de admissão demonstra uma estenose severa do extremo proximal do conduto de Sano, com diâmetro não superior a 1,3 mm e gradiente sistólica máxima de 80 mmHg.
Decide-se realizar cateterismo cardíaco de urgência para implantar um stent na união entre o ventrículo direito e o conduto de Sano, mas devido à gravidade da paciente, que requer doses elevadas de drogas vasoativas para manter pressões sistólicas elevadas e assim alcançar um fluxo pulmonar aceitável, decide-se realizar o procedimento com a paciente em ECMO venoarterial. A paciente é trasladada a nosso serviço de Hemodinâmica, onde é entubada com cânulas de 14 Fr na veia jugular interna direita e de 10 Fr na artéria carótida comum direita. O resto do procedimento hemodinâmico é feito com 80% de bypass. O registro basal de pressões mostra uma pressão média de aurícula direita de 6 mmHg, de ventrículo direito de 66/10 mmHg e de artérias pulmonares de 12/10 (11) mmHg. Não havia gradiente de pressão entre o ventrículo direito e a neoaorta. Em termos angiográficos, identifica-se uma estenose complexa do conduto de Sano com um diâmetro no nível da anastomose proximal do conduto de 1,5 mm associada a uma estenose severa no nível da anastomose distal do conduto e à origem da artéria pulmonar direita com diâmetros de 1 a 1,5 mm (figura 1 e 2). É feita uma angioplastia com balão Armada, de 6 mm de diâmetro por 2 cm de comprimento da artéria pulmonar direita e anastomose distal do conduto de Sano (figura 2). Posteriormente é implantado stent Palmaz Blue, de 5 mm de diâmetro por 18 mm de comprimento no extremo proximal do conduto (figura 3). Após as intervenções houve uma melhora significativa da oxigenação e um aumento da pulsatilidade da pressão nas artérias pulmonares (artéria pulmonar direita: 20/11 mmHg com média de 16 mmHg). Consegue-se suspender a norepinefrina, retirar a ECMO-VA na sala de hemodinâmica e a paciente é transferida à Unidade de Paciente Crítico Cardiovascular de nossa instituição. Posteriormente ao procedimento sua evolução foi favorável, tendo sido suspensas as drogas vasoativas 7 horas após o mesmo, e tendo sido retirada a ventilação mecânica e a extubação 24 horas após o procedimento. A paciente recebeu alta 3 dias após o procedimento.
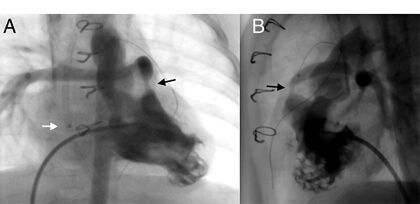
Figura 1. Ventriculografia direita em projeção AP (A) e lateral (B), a flecha negra indica a estenose severa no extremo proximal do conduto de Sano de 1,5 mm a partir da parede anterior do ventrículo direito. A flecha branca indica a marca radiopaca do extremo distal da cânula venosa da ECMO.
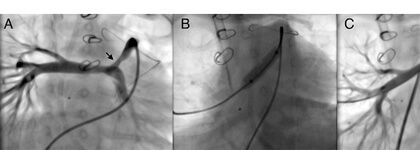
Figura 2. Angiografia seletiva no conduto de Sano em projeção caudal que demonstra uma zona de estenose severa no extremo distal do conduto de 1,4 mm associada à estenose de origem do ramo direito de 2,8 mm (A). Imagem fluoroscópica durante angioplastia com cateter balão Armada® 6 mm x 2 cm (B) e resultado angiográfico final (C).
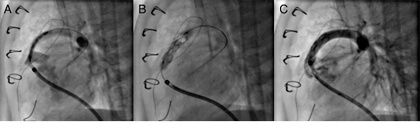
Figura 3. Imagens durante o procedimento mostrando o posicionamento do stent Palmaz Blue® de 6 x 18 mm no extremo proximal do conduto de Sano A), o deslocamento do stent durante a insuflação do cateter balão (B) e o resultado angiográfico final favorável (C).
Comentário
O caso clínico aqui apresentado é um exemplo de um procedimento intervencionista realizado em um recém-nascido no pós-operatório de uma cirurgia cardíaca complexa e com uma lesão residual significativa. A intervenção realizada pode ser hemodinamicamente mal tolerada, motivo pelo qual se decidiu realizá-la com apoio de uma assistência circulatória com ECMO (extra corporeal membrane oxygenation). A incorporação da ECMO como recurso terapêutico para os pacientes com cardiopatias em sua estabilização pré ou pós-operatória conduziu a novos cenários clínicos. Um deles é a necessidade de transferir os pacientes afetados ao laboratório de hemodinâmica e a realização de procedimentos intervencionistas durante a assistência circulatória na ECMO.
A realização de cateterismos cardíacos em pacientes conectados a ECMO implica uma preparação, organização e logística particular, dada a instabilidade deste tipo de pacientes e à complexidade dos traslados. Apesar do anteriormente afirmado, a experiência publicada demonstrou que é possível realizar ditos procedimentos de forma segura (1, 2). Adicionalmente, demonstrou-se que as intervenções realizadas precocemente em pacientes com cardiopatias operados estando conectados a ECMO se traduzem em melhor prognóstico e sobrevida no memento da alta (3 -5).
A instituição da ECMO como medida de estabilização prévia a um cateterismo intervencionista é uma opção para a realização de um procedimento em condições de maior segurança, como se fez no caso aqui apresentado, realizando angioplastia com stent em um conduto de Sano com estenose severa, convertendo assim uma situação clínica instável em uma situação controlada.
A estenose de um conduto de Sano em pacientes após a cirurgia de Norwood é uma complicação conhecida, relatada entre 16% e 24% dos pacientes (6 - 8). Já há relatos sobre a possibilidade de corrigir dita lesão utilizando angioplastia com stent no conduto de Sano, o que costuma resultar em uma alta taxa de sucesso com melhora da saturação de oxigênio destes pacientes (9,10). No caso aqui relatado, a angioplastia foi bem-sucedida com uma melhora de todos os parâmetros. Este é um procedimento altamente efetivo que usualmente se realiza em recém-nascidos com hipoxemia significativa. A estabilidade destes pacientes e a segurança do procedimento pode ser melhorada ao conectá-los a ECMO, sendo esta uma estratégia razoável e segura para este particular tipo de pacientes (10,11).
_
Referências Bibliográficas
- Boscamp NS, Turner ME, Crystal M, Anderson B, Vincent JA, Torres AJ. Cardiac Catheterization in Pediatric Patients Supported by Extracorporeal Membrane Oxygenation: A 15-Year Experience. Pediatr Cardiol. 2017; 38(2):332-337.
- Panda BR, Alphonso N, Govindasamy M, Anderson B, Stocker C, Karl TR. Cardiac catheter procedures during extracorporeal life support: a risk-benefit analysis. World J Pediatr Congenit Heart Surg. 2014; 5(1):31-7.
- Abraham BP, Gilliam E, Kim DW, Wolf MJ, Vincent RN, Petit CJ. Early catheterization after initiation of extracorporeal membrane oxygenation support in children is associated with improved survival. Catheter Cardiovasc Interv. 2016; 88(4):592-599.
- Burke CR, Chan T, Rubio AE, McMullan DM. Early Cardiac Catheterization Leads to Shortened Pediatric Extracorporeal Membrane Oxygenation Run Duration. J Interv Cardiol. 2017; 30(2):170-176.
- Kato A, Lo Rito M, Lee KJ, Haller C, Guerguerian AM, Sivarajan VB, Honjo O. Impacts of early cardiac catheterization for children with congenital heart disease supported by extracorporeal membrane oxygenation. Catheter Cardiovasc Interv. 2017; 89(5):898-905.
- Nigro JJ, Bart RD, Derby CD, Sklansky MS, Starnes VA. Proximal conduit obstruction after Sano modified Norwood procedure. Ann Thorac Surg. 2005; 80(5):1924-8.
- Gray RG, Minich LL, Weng HY, Heywood MC, Burch PT, Cowley CG. Effect of endovascular stenting of right ventricle to pulmonary artery conduit stenosis in infants with hypoplastic left heart syndrome on stage II outcomes. Am J Cardiol. 2012;110(1):118-23.
- Münsterer A, Kasnar-Samprec J, Hörer J, Cleuziou J, Eicken A, Malcic I, Lange R, Schreiber C. Treatment of right ventricle to pulmonary artery conduit stenosis in infants with hypoplastic left heart syndrome. Eur J Cardiothorac Surg. 2013; 44(3):468-71
- Dähnert I, Riede FT, Razek V, Weidenbach M, Rastan A, Walther T, Kostelka M. Catheter interventional treatment of Sano shunt obstruction in patients following modified Norwood palliation for hypoplastic left heart syndrome. Clin Res Cardiol. 2007; 96(10):719-22.
- Muyskens S, Nicolas R, Foerster S, Balzer D. Endovascular stent placement for right ventricle to pulmonary artery conduit stenosis in the Norwood with Sano modification. Congenit Heart Dis. 2008;3(3):185-90.
- Gulgun M, Slack M. Stent Placement in a Neonate with Sano Modification of the Norwood using Semi-Elective Extracorporeal Membrane Oxygenation. Arq Bras Cardiol. 2016; 107(6):600-604.
Conflito de interesses: Nenhum.




