Acesso transaórtico
*Autor para correspondência: Dr. César Morís, cmoris@uniovi.es
A estenose aórtica (EA) é a valvoplastia cardíaca mais frequente nos países desenvolvidos. Sua prevalência aumenta progressivamente com a idade, de 0,2% aos 50-59 anos a 1,3% aos 60-69, 3,9% aos 70-79 e até 9,8% aos 80-89 anos. O implante percutâneo da valva aórtica (TAVI) revolucionou o tratamento da EA. Atualmente está disponível em 65 países e foram realizados mais de 250.000 implantes, 70.000 dos quais em 2015, embora se estime que dita cifra se quadruplicará até superar os 280.000 em 2025. O TAVI é atualmente o tratamento de escolha para os pacientes com EA inoperável e a opção terapêutica preferida para os pacientes de alto risco[1-3].
O acesso retrógrado transfemoral é o mais frequentemente utilizado, fato impulsionado pela progressiva diminuição do calibre dos sistemas de liberação e sua maior flexibilidade, sendo utilizado em mais de 90% dos casos atuais. Mas ainda há um pequeno número de pacientes nos quais o acesso pela via femoral não é possível e, nesses casos, podem ser avaliados acessos alternativos como a via transapical, transubclávia, transcarotídea, transcava e aórtica direta (AD).
Três recentes registros demonstram que o acesso transfemoral tem uma taxa significativamente menor de mortalidade em 30 dias [OR: 0,56 (0,5-0,64)] e em um ano (OR 0,68, 0,60-0,75), em comparação com o acesso não transfemoral [4-6].
Com relação aos acessos não femorais, há alguns meses, Takahide Arai e colaboradores publicaram um estudo descritivo no qual se compara o acesso transfemoral com o transaórtico e com o transapical para TAVI, mostrando maior mortalidade em 30 dias e em um ano no grupo transapical. Os autores concluíram que a via transaórtica pode ser considerada uma alternativa segura ao acesso transfemoral[7]. Nesse sentido e abundando nos bons resultados do acesso aórtico direto, recentemente relataram os dados referentes à maior coorte até o momento, na qual se descreve uma mortalidade em 30 dias de 6,1%[8].
As peculiaridades de cada um dos acessos vasculares para o TAVI tornam necessário avaliar cuidadosamente a carga aterosclerótica, o tamanho da artéria e sua tortuosidade, assim como a presença de trombos murais.
Atualmente estão em andamento vários ensaios clínicos e em um futuro próximo as indicações para os acessos alternativos ao femoral provavelmente estejam definidas de maneira mais precisas e estendidas a um espectro mais amplo de candidatos a TAVI.
PASSO A PASSO
O acesso transaórtico pode ser conduzido mediante uma miniesternotomia em “J” (Figura 1A) ou uma minitoracotomia direita.
- Miniesternotomia em “J”
Faz-se uma incisão cutânea na linha média de 5 a 6 cm da jugular esternal até o nível da terceira costela. Com uma pequena serra oscilante realiza-se a esternotomia até o segundo ou o terceiro espaço intercostal no lado direito. Mantém-se o pericárdio distanciado e expõe-se a aorta ascendente.
- Minitoracotomia direita.
Faz-se uma incisão cutânea de 4 cm na paraesternal direita. A pleura é recolhida e a exposição da aorta ascendente é alcançada com a utilização de um retrator de tecido mole e/ou um pequeno separador de costelas. O pericárdio é identificado, secciona-se paralelamente a incisão cutânea provocando retração.
Ambos os acessos permitem expor a porção proximal da aorta ascendente, mas selecionar o acesso torácico correto é importante para cada paciente e a decisão diz respeito tanto a características técnicas quanto de factibilidade de acesso.
A toracotomia será utilizada quando a aorta ascendente estiver horizontalizada, encontrar-se dirigida à direita e estiver situada abaixo da caixa torácica. Ao contrário, a esternotomia será a opção adequada quando a aorta estiver na linha média, for mais profunda e seu trajeto for vertical [2-3]. Outros condicionantes são que enquanto a esternotomia preserva a pleura intacta e geralmente oferece um maior campo da aorta, a toracotomia evita as pontes coronarianas permeáveis – se houver (geralmente do lado esquerdo da aorta).
Uma vez exposta a aorta, o pericárdio é costurado nas bordas da pele, criando uma cunha e mantendo separados os tecidos pulmonares e mediastinais. São feitas, então, na parede aórtica, duas suturas concêntricas de polipropileno 3-0 no ponto de inserção desejado, em “bolsa de tabaco”, e realiza-se punção do centro das suturas com uma agulha padrão. A seguir, coloca-se um introdutor de 6 french com um fio-guia de 0,035” de ponta J (Figura 1B).
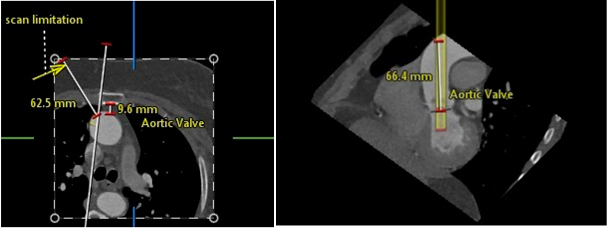
Um dos aspectos mais importantes desse acesso é a distância entre a punção na aorta e o plano valvar aórtico, já que deve haver distância suficiente para alojar a valva durante a liberação. Para estabelecer dita altura, mede-se previamente sobre a tomografia computadorizada (Figura 2) e durante o procedimento se utiliza um cateter pigtail centimetrado situado na aorta ascendente e, por radioscopia, assinala-se a altura da punção, que deve estar pelo menos a 6 cm de distância do anel.
Através do introdutor, cruza-se a valva aórtica, situa-se o fio-guia de alto suporte no ventrículo esquerdo, insere-se o introdutor escolhido para o implante da prótese, que é realizado de forma habitual. A curta distância entre o anel e a punção, assim como a falta de roce com o arco aórtico, facilitam a inserção da valva e encurtam a curva de aprendizagem do operador. Após a liberação da valva, as suturas da bolsa são costuradas sob visão direta, de forma similar à descanulação após a circulação extracorpórea. O fechamento da parede torácica se realiza com a prática cirúrgica padrão.
O acesso aórtico direto, apesar do caráter invasivo da minitoracotomia e da aortotomia, tem várias vantagens. Trata-se de uma via de acesso tecnicamente factível, familiar e fácil de compreender para os cirurgiões cardíacos. Além disso, associou-se com resultados favoráveis e uma menor taxa de complicações (sangramento, risco de lesão miocárdica) e menor duração da estadia na unidade de terapia intensiva em comparação com o acesso transapical. As vantagens em relação às abordagens transfemorais ou transaxilares incluem eludir artérias menores (íliofemoral ou subclávia) por inserção direta da bainha na aorta, o que reduz o risco de complicações. Ademais, a aproximação à valva aórtica se dá, em alguns casos, em uma linha reta direta, o que facilita o posicionamento da valva, particularmente em uma raiz de aorta horizontal [4-6].
FIGURA 1. (A) Incisão para o acesso transaórtico direto mediante miniesternotomia. (B) Exposição da aorta ascendente mediante uma minitoracotomia. Mostra-se a inserção de um introdutor através da aortotomia com progressão de um fio-guia de alto suporte.
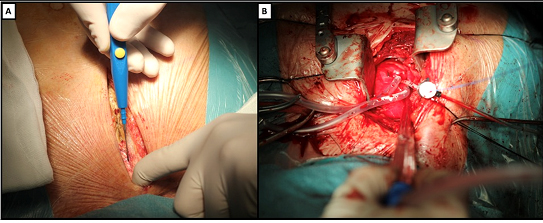
FIGURA 2. Estudo de tomografia computadorizada no qual se pode ver à esquerda em um corte axial a relação da aorta com o esterno e um possível acesso por toracotomia direita (flecha). À direita, pode-se ver o ponto teórico de punção da aorta a uma distância de 6,6 mm do anel valvar aórtico.
REFERÊNCIAS
- Edwards FH, Peterson ED, Coombs LP et al. Prediction of operative mortality after valve replacement surgery. J Am Coll Cardiol 2001;37(3):885-892.
- Bapat VN, Bruschi G. Transaortic access is the key to success. EuroIntervention 2013;9 Suppl:S25-S32.
- Bruschi G, De MF, Botta L et al. Direct aortic access for transcatheter self-expanding aortic bioprosthetic valves implantation. Ann Thorac Surg 2012;94(2):497-503.
- Wendler O, Schymik G, Treede H, et al. SOURCE 3 Registry: Design and 30-Day Results of the European Post Approval Registry of the Latest Generation of the Sapien 3TM Transcatheter. Circulation. 2017;CIRCULATIONAHA. January 19, 2017 DOI:10.1161/CIRCULATIONAHA.116.025103.
- Kalra S, Firoozi S, Yeh J et al. Initial Experience of a Second-Generation self-Expanding Transcatheter Aortic Valve The UK & Ireland Evolut R Implanters’ Registry. J Am Coll Cardiol Intv 2017;10:276–82.
- Popma J, Reardon R, Khabbaz K. Early Clinical Outcomes After Transcatheter Aortic Valve Replacement Using a Novel Self-Expanding Bioprosthesis in Patients With Severe Aortic Stenosis Who Are Suboptimal for Surgery Results of the Evolut R U.S. Study. J Am Coll Cardiol Intv 2017;10:268–75.
- Arai T, Romano M, Lefevre T et al. Direct Comparison of Feasibility and Safety of Transfemoral Versus Transaortic Versus Transapical Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv 2016;9(22):2320-2325.
- Bapat V, Frank D, Cocchieri R et al. Transcatheter Aortic Valve Replacement Using Transaortic Access: Experience From the Multicenter, Multinational, Prospective ROUTE Registry. JACC Cardiovasc Interv 2016;9(17):1815-1822.


