Desde o primeiro implante percutâneo da valva aórtica (TAVI) realizado em 2002 pelo Dr. Alan Cribier, em Ruan, França[1], o número de procedimentos aumentou exponencialmente.
A evolução dos sistemas de liberação, os quais podem ser inseridos por introdutores de menor tamanho (14 Fr para válvulas CoreValve Evolut R® e Sapien® 3) contribuiu para a diminuição de complicações vasculares[2,3]. No entanto, existe um limitado número de pacientes nos quais não se pode realizar este procedimento pelo acesso arterial convencional (femoral) ou por acessos alternativos tradicionais como o subclávio e axilar[4], o aórtico direto[5], o transapical[6], o transcarotídeo[7] e o supraesternal[8].
A via transcava[9] surge como uma alternativa viável para a realização do implante percutâneo da valva aórtica neste tipo de pacientes.
Greenbaum et al[11], em 2016 deram a conhecer um estudo observacional com 100 pacientes que foram submetidos ao implante valvar aórtico por via transcava. O acesso vascular foi bem-sucedido em 99 de 100 sujeitos e o sucesso com o dispositivo de oclusão (AmplatzerTM) foi de 98/99. Um dos casos requereu implante de stent recoberto. A sobrevida após a alta hospitalar foi de 96% e a sobrevida em 30 dias foi de 92%. As complicações vasculares maiores associadas ao acesso foram de 13%. A média de estadia hospitalar foi de 4 dias.
Pode-se concluir que a via de acesso transcava para implante percutâneo da valva aórtica é uma alternativa que exige uma adequada planificação do procedimento e que é possível realizá-lo em pacientes com risco proibitivo ou alto para cirurgia convencional por presença de contraindicações ou por múltiplas comorbidades e deficientes acessos vasculares convencionais e alternativos. A complicação mais temida associada ao procedimento é o sangramento retroperitoneal que pode ocorrer em ao redor de 1 a 2% dos casos.
PASSO A PASSO
Para escolher a via trancava é necessário fazer uma tomografia multicorte (TC) de tórax e abdómen que permita avaliar as artérias subclávias, aorta, ilíacas e femorais, a relação aorto-cava e identificar o ponto mais indicado para realizar a punção cava.
Lederman et al. sugerem que se deve escolher o ponto onde houver menor quantidade de cálcio, sem estruturas interpostas (intestino). Deve-se realizar a punção a uma distância prudente da artéria renal, da veia renal, dos vasos mesentéricos e da bifurcação aortoilíaca, para o caso de ser necessário o uso de stent recoberto. A figura 1 resume as recomendações para a escolha do ponto de punção[10].
Procedimento:
Com o cateter preposicionado, deve-se realizar uma injeção simultânea de meio de contraste na veia cava inferior e na aorta a fim de localizar o ponto de punção por fluoroscopia. Uma vez localizado o ponto de punção, introduz-se por via arterial um fio-guia laço e alinha-se com o cateter previamente posicionado na veia cava inferior (cateter guia renal) em duas projeções (usualmente RAO 30° e LAO 60°), com o fim de que o fio-guia a inserir faça um efeito de alvo sobre o laço deslocado. Introduz-se um fio-guia de um só corpo metálico sem recobrimento hidrofílico de ponta rígida (0,014” ou 0,018”) de 260 cm ou 300 cm, o qual vai conectado em seu extremo proximal a um eletro-bisturi para que a passagem pelas estruturas seja facilitada pelo corte.
Já no lúmen aórtico, retira-se o eletro-bisturi e enlaça-se o fio-guia rumo ao arco aórtico. Procede-se a realizar dilatações da união cavo-aórtica com um balão 2,5 a 3,0 mm que tenha possibilidade de intercambiar o fio-guia 0,014” ou 0,018 por um 0,035” de alto suporte. Através deste último, avança-se o introdutor 18 F da valva percutânea. Uma vez posicionado o extremo distal do introdutor na aorta abdominal, realiza-se o procedimento de implante valvar percutâneo da mesma forma que por um acesso arterial femoral tradicional.
Depois de realizado o implante da valva, deve-se proceder a ocluir o shunt arteriovenoso com um dispositivo de oclusão tipo AmplatzerTM (AGA Medical Corporation). É preferível que se utilize o de comunicação interventricular Nº 8 (9-VSD-MUSC-008). Injeta-se meio de contraste para descartar vazamentos retroperitoneais que, caso se apresentem, recomenda-se insuflação de balão complacente utilizado na pós-dilatação da endoprótese para a oclusão temporal das estruturas vasculares. Caso o vazamento retroperitoneal persista, sugere-se o uso de stent recoberto em aorta. Uma vez descartada a presença de vazamentos, retiram-se os introdutores. FIGURA 2[9]
FIGURA 1: Recomendações para a escolha do ponto de punção
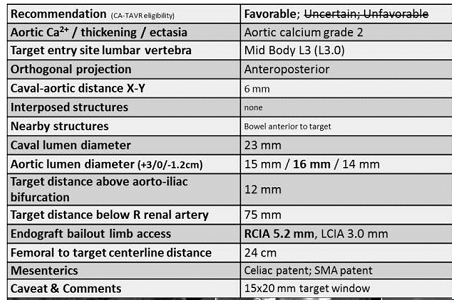
Catheter Cardiovasc Interv. 2015 Dec 1; 86(7): 1242–1254.
FIGURA 2
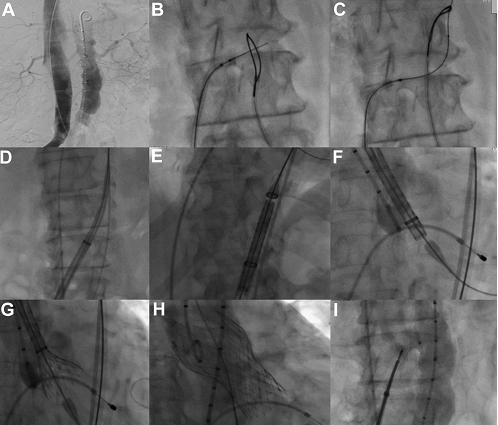
(A) Flebografia e aortografia antes do procedimento; (B) Fio-guia Confiança Pro 12 entrando no laço na aorta; 9C) Fio-guia capturado pelo laço e inserido na aorta ascendente; (D) Introdutor 18-F a partir do acesso venoso que conecta a veia femoral à aorta; (E F) Medtronic CoreValve ReValving™ sendo inserido no trato de saída do ventrículo esquerdo; (G e H) Liberação da prótese; e (I) oclusão da fístula cavo-aórtica com dispositivo AmplatzerTM Muscular VSD Occluder.
JACC Cardiovascular Interventions Sep 2014, 7 (9) 1075-1077.
BIBLIOGRAFIA
- Cribier A, Eltchaninoff H, Bash A, Borenstein N, Tron C, Bauer F, et al. Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description. Circulation. 2002;106:3006-8.
- John Webb, MD, Gino Gerosa, MD, Thierry Lefèvre, MD, Jonathon Leipsic, MD, Mark Spence, MD, Martyn Thomas, MD…..Thomas Walther, MD et al, Thirty-day Outcome Following CoreValve Evolut R Transcatheter Aortic Valve Implantation: An All-comers Prospective Study. JACC 64, NO. 21,2014. http://dx.doi.org/10.1016/j.jacc.2014.09.026
- Nils Perrin, Marco Roffi, Angela Frei, Anne-Lise Hachulla, Christoph Ellenberger, Hajo Müller, Mustafa Cikirikcioglu, Marc Licker, Stephane Noble. Thirty-day Outcome Following CoreValve Evolut R Transcatheter Aortic Valve Implantation: An All-comers Prospective Study. Revista Española de cardiología 2016. DOI:1016/j.rec.2016.11.024.
- Ribeiro, Henrique Barbosa, & Rodés-Cabau, Josep. (2012). Trans-subclavian access in transcatheter aortic valve implantation (TAVI): an elegant alternative for non-ideal candidates to the transfemoral access method.Revista Brasileira de Cardiologia Invasiva, 20(3), 233-235. https://dx.doi.org/10.1590/S2179-83972012000300003.
- Bapat, V., Khawaja, M. Z., Attia, R., Narayana, A., Wilson, K., Macgillivray, K., Young, C., Hancock, J., Redwood, S. and Thomas, M. (2012), Transaortic transcatheter aortic valve implantation using edwards sapien valve. Cathet. Cardiovasc. Intervent., 79: 733–740. doi:10.1002/ccd.23276
- Jörg Kempfert, Ardawan J. Rastan, Friedrich-W. Mohr, Thomas Walther; A new self-expanding transcatheter aortic valve for transapical implantation — first in man implantation of the JenaValve™.Eur J Cardiothorac Surg 2011; 40 (3): 761-763. doi: 10.1016/j.ejcts.2010.12.063
- Alexandre Azmoun, Nicolas Amabile, Ramzi Ramadan, Saïd Ghostine, Christophe Caussin, Sahbi Fradi, François Raoux, Philippe Brenot, Remi Nottin, Philippe Deleuze; Transcatheter aortic valve implantation through carotid artery access under local anaesthesia.Eur J Cardiothorac Surg, 2014; 46 (4): 693-698. doi: 10.1093/ejcts/ezt619
- Andy C. Kiser, William W. O'Neill, Eduardo de Marchena, Richard Stack, Mauricio Zarate, Antonio Dager, Michael Reardon; Suprasternal direct aortic approach transcatheter aortic valve replacement avoids sternotomy and thoracotomy: first-in-man experience. Eur J Cardiothorac Surg, 2015; 48 (5): 778-784. doi: 10.1093/ejcts/ezu524.
- Pedro O.Martinez-Clark, Vikas Singh, Jairo A. Cadena, Angela Maria Cucalon Reyes, Cesia Gallegos, Antonio Dager, Adam Greenbaum William W. O’Neill ; Transcaval Retrograde Transcatheter Aortic Valve Replacement for Patients With No Other Access First-in-Man Experience With CoreValve ; JACC: Cardiovascular Interventions Sep 2014, 7 (9) 1075-1077; DOI: 1016/j.jcin.2014.03.008
- Lederman, R. J., Babaliaros, V. C., & Greenbaum, A. B. (2015). How to Perform Transcaval Access and Closure for Transcatheter Aortic Valve Implantation.Catheterization and Cardiovascular Interventions : Official Journal of the Society for Cardiac Angiography & Interventions, 86(7), 1242–1254. http://doi.org/10.1002/ccd.26141
- Adam B. Greenbaum, Vasilis C. Babaliaros, Marcus Y. Chen, Annette M.Stine, Toby Rogers, William. O’Neill, Gaetano Paone, Vinod H. Thourani, Kamran I. Muhammad, Robert A. Leonardi, Stephen Ramee, James F.Troendle, Robert J. Lederman ; Transcaval Access and Closure for Transcatheter Aortic Valve Replacement: A Prospective Investigation ; Journal of the American College of Cardiology, Oct 2016, 23129; DOI: 10.1016/j.jacc.2016.10.024
