O implante de stents na via de saída do ventrículo direito (VSVD) pode ser empregado em inúmeras situações com necessidade de ampliação do fluxo proveniente do ventrículo direito para as artérias pulmonares. Neonatos com quadros de hipoxemia (1-3), no pós-operatório imediato de ampliação da VSVD em pacientes com grave situação hemodinâmica e no pós-operatório tardio de cirurgias com ampliação da VSVD com conduto ou patch transanular (4, 5) para preparo destas vias de saída para implante percutâneo de valvas pulmonares (6-10). Esta última será nosso escopo principal.
Abaixo demonstramos os passos para o implante de stents para este fim:
- Anestesia geral: São procedimentos longos, com grande manipulação de cateteres e necessidade de trocas de introdutores podendo gerar desconforto ao paciente que pode mudar de posição com perda dos parâmetros obtidos para o posicionamento do stent;
- Múltiplas angiografias: Devem ser realizadas para permitir medidas acuradas dos diâmetros e comprimentos da via de saída. As projeções OAD cranial e perfil esquerdo geralmente são as ideais. Para a injeção em perfil esquerdo os braços devem ser posicionados para cima, facilitando a visualização adequada;
- Aortografia e teste de compressão coronariana: Em todos os pacientes candidatos ao implante de stent na VSVD o teste de compressão coronariana deve ser realizado com a insuflação do balão no diâmetro desejado e aortografia concomitante. Diversas projeções podem ser realizadas para avaliar a proximidade da artéria coronária. As projeções caudal (OAE ou PA) e perfil esquerdo geralmente demonstram se existe risco de compressão com o implante definitivo do stent (Figuras 1 e 2);
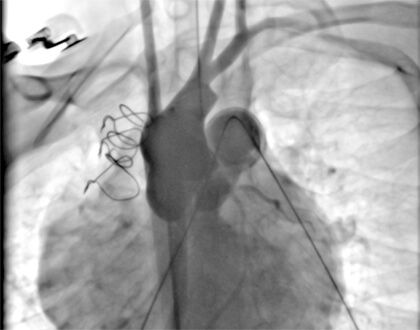
Figura 1
Teste de compressão coronariana em projeção perfil esquerdo: balão insuflado na VSVD e aortografia concomitante mostrando fluxo coronário adequado.
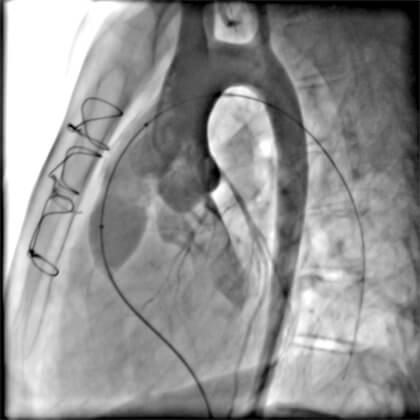
Figura 2
Teste de compressão coronariana em projeção OAE caudal: balão insuflado na VSVD e aortografia concomitante mostrando proximidade da artéria descendente anterior porém com fluxo adequado.
- Posicionamento do tubo para implante: Deve ser escolhida uma projeção ideal para o implante dependendo da anatomia e da preferência do operador. Geralmente a projeção perfil esquerdo permite visualização de toda a via de saída e a OAD cranial auxilia a posicionar o stent abaixo da bifurcação das artérias pulmonares;
- Posicionamento do fio-guia para implante: É um dos passos primordiais para o sucesso do procedimento. Utilizamos sempre guias 0,035" extra-stiff posicionados na região mais distal e inferior da artéria pulmonar escolhida. A maioria das vezes a artéria pulmonar esquerda é escolhida porém em algumas variações anatômicas nativas ou após manipulação cirúrgica a artéria pulmonar direita pode ser a melhor opção. Com o auxílio do cateter Judkins direito, Multipurpose ou Wedge® e fio-guia hidrofílico 0,035", a artéria é cateterizada e após a obtenção do local ideal este é trocado pelo fio-guia extra-stiff escolhido. Cuidado extra deve ser tomado para não perder o posicionamento e para evitar trauma vascular associado;
- Posicionamento da bainha de Mullins: A bainha compatível com o conjunto balão-stent é avançada ultrapassando o local de implante. O seu posicionamento permite ao operador antever como será o avanço do stent. A bainha do tipo aramada deve ser utilizada principalmente nas anatomias mais complexas com múltiplas curvas na VSVD e artérias pulmonares;
- Escolha do balão e stent: O stent implantado deve ter dimensões para cobrir totalmente a via de saída ou conduto com diâmetro suficiente para evitar migração. A VSVD dos pacientes submetidos a patch transanular geralmente é dilatada podendo atingir diâmetros maiores que 25 mm. Poucas opções de stents disponíveis na América Latina permitem dilatação até este tamanho, tornando o procedimento inviável nestas situações. Para aqueles pacientes portadores de conduto VD-TP o ideal é conhecer de antemão o diâmetro pois muitas vezes existe intensa calcificação do tubo e suas dimensões são menores que as reais. Para estes casos a dilatação prévia com cateter-balão no sentido de "testar" a complacência com diâmetros progressivamente maiores deve ser realizada. Devido ao risco de fratura da VSVD o ideal é sempre ter um stent coberto de backup para uma eventual situação de emergência. Novas angiografias devem ser realizadas após cada insuflação do balão, evitando ampliar eventuais linhas de dissecção;
- Posicionamento e implante do stent: O conjunto balão-stent é avançado sobre o fio-guia e posicionado na VSVD de acordo com a angiografia prévia. Deve-se sempre observar se o stent esta bem posicionado sobre o balão antes de retirar a bainha. Através da bainha podem ser realizadas angiografias para ajuste antes de expor totalmente o stent e também após o implante do mesmo. O manômetro deve ser utilizado para insuflação respeitando os limites de pressão de cada balão;
- Angiografias finais: Após o implante novas angiografias são realizadas com o uso de cateteres diversos como o Multitrack® ou pigtail (Figuras 3 e 4). A desvantagem deste último é a necessidade de ter de retirar o fio-guia da artéria pulmonar;
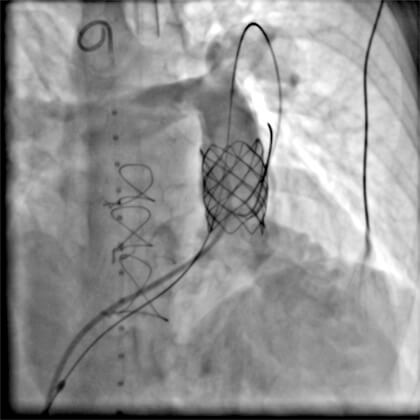
Figura 3
Angiografia pós implante em perfil esquerdo: stent bem aposto na VSVD cobrindo toda a sua extensão.
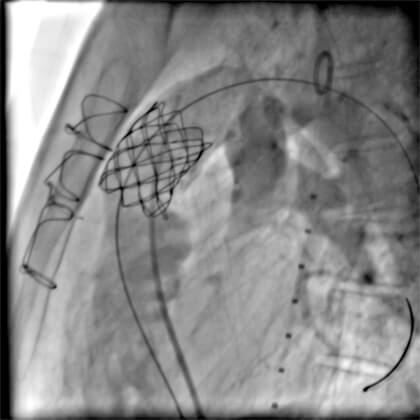
Figura 4
Angiografia pós implante em projeção OAE cranial: stent bem aposto na VSVD com
- Retirada do fio-guia extra-stiff: Este é um passo importante devendo ser realizada com cuidado avançando cateter pelo guia e substituindo o mesmo por hidrofílico, evitando o deslocamento do stent recém implantado;
- Retirada do introdutor e hemostasia: Devido as dimensões do introdutor utilizado podem ser posicionados dispositivos de sutura do vaso (Perclose®, por exemplo). Sutura em "8" ou compressão hemostática também são efetivas para atingir a hemostasia adequada.
_
Referências:
- Dohlen G, Chaturvedi RR, Benson LN, Ozawa A, Van Arsdell GS, Fruitman DS, et al. Stenting of the right ventricular outflow tract in the symptomatic infant with tetralogy of Fallot. Heart. 2009;95(2):142-7.
- Bertram H, Emmel M, Ewert P, Grohmann J, Haas NA, Jux C, et al. Stenting of Native Right Ventricular Outflow Tract Obstructions in Symptomatic Infants. Journal of interventional cardiology. 2015;28(3):279-87.
- Barron DJ, Ramchandani B, Murala J, Stumper O, De Giovanni JV, Jones TJ, et al. Surgery following primary right ventricular outflow tract stenting for Fallot's tetralogy and variants: rehabilitation of small pulmonary arteries. European journal of cardio-thoracic surgery. 2013;44(4):656-62.
- Boudjemline Y, Sarquella-Brugada G, Kamache I, Patel M, Ladouceur M, Bonnet D, et al. Impact of right ventricular outflow tract size and substrate on outcomes of percutaneous pulmonary valve implantation. Archives of cardiovascular diseases. 2013;106(1):19-26.
- Malekzadeh-Milani S, Ladouceur M, Cohen S, Iserin L, Boudjemline Y. Results of transcatheter pulmonary valvulation in native or patched right ventricular outflow tracts. Archives of cardiovascular diseases. 2014;107(11):592-8.
- Nordmeyer J, Lurz P, Khambadkone S, Schievano S, Jones A, McElhinney DB, et al. Pre-stenting with a bare metal stent before percutaneous pulmonary valve implantation: acute and 1-year outcomes. Heart. 2011;97(2):118-23.
- Demkow M, Biernacka EK, Spiewak M, Kowalski M, Siudalska H, Wolski P, et al. Percutaneous pulmonary valve implantation preceded by routine prestenting with a bare metal stent. Catheterization and cardiovascular interventions. 2011;77(3):381-9.
- Cardoso R, Ansari M, Garcia D, Sandhu S, Brinster D, Piazza N. Prestenting for prevention of melody valve stent fractures: A systematic review and meta-analysis. Catheterization and cardiovascular interventions. 2016;87(3):534-9.
- McElhinney DB, Cheatham JP, Jones TK, Lock JE, Vincent JA, Zahn EM, et al. Stent fracture, valve dysfunction, and right ventricular outflow tract reintervention after transcatheter pulmonary valve implantation: patient-related and procedural risk factors in the US Melody Valve Trial. Circulation Cardiovascular interventions. 2011;4(6):602-14.
- Bishnoi RN, Jones TK, Kreutzer J, Ringel RE. NuMED Covered Cheatham-Platinum Stent for the treatment or prevention of right ventricular outflow tract conduit disruption during transcatheter pulmonary valve replacement. Catheterization and cardiovascular interventions. 2015;85(3):421-7.