Papel da Valvoplastia Aórtica no TAVI
Desde que Alain Cribier relatou sua primeira experiência com o implante percutâneo da valva aórtica (TAVI), a valvoplastia aórtica com balão (VAB) se impôs como um passo prévio obrigatório para assegurar a passagem e a expansão da prótese em valvas nativas severamente calcificadas e estenóticas e, por sua vez, evitar o potencial comprometimento hemodinâmico durante o posicionamento.
Esta situação não foi questionada inicialmente, em parte devido ao alto perfil dos sistemas de primeira geração disponíveis, como a Edwards Sapien (Edwards LifeSience) de 22 e 24 Fr, e a primeira CoreValve (Medtronic) de 24 Fr.
O grande desenvolvimento tecnológico na primeira década permitiu a disponibilidade de sistemas mais flexíveis e de menor perfil. Começou-se, então, a questionar a necessidade da VAB, apareceu a primeira experiência com implante direto (sem VAB prévia) com CoreValve de 18(1) Fr e Sapien XT(2) e a ser reconhecida mais claramente a potencial morbidade associada à pré-dilatação.
_
Risco/Benefício da Valvoplastia Aórtica com Balão
A VAB está longe de ser um procedimento inócuo. Durante mais de duas décadas foi utilizada como tratamento paliativo ou como ponte para a substituição cirúrgica e essa experiência mostra uma mensurável taxa de complicações específicas: 1,5% de morte, 18% de AVC(3), 0,3% de ruptura do anel, 1,1% de insuficiência aórtica severa(4). Em estudos comparativos de TAVI com e sem VAB prévia, a ocorrência de novo bloqueio do ramo esquerdo e bloqueio AV completo foi mais frequente em 30 dias e mais persistentes em um ano quando se realizou VAB previamente ao implante(5).
Menos presente nos estudos mas evidente do ponto de vista da experiência, a VAB pode ser muito mal tolerada em pacientes com deterioro severo da função ventricular e/ou hipertensão pulmonar.
Por outro lado, a VAB proporciona informação relevante acerca do comportamento das valvas nas anatomias com raiz estreita quando a distância do anel aos óstios coronarianos não supera os 12 mm e o risco de oclusão é alto. Também se especulou a respeito da maior incidência de pós-dilatação (e suas complicações específicas associadas) quando o implante é direto, sem VAB prévia.
_
Estudos comparativos entre TAVI “direto” versus VAB prévio
Podemos evitar a morbidade associada à VAB implantando a válvula diretamente?
Embora esta questão tenha suscitado considerável interesse, a maior parte da experiência provém de publicações de casuísticas de um único centro, em geral com escasso número de pacientes.
Duas recentes revisões sistemáticas da literatura aportaram valiosa informação neste contexto.
Na primeira delas, Bagur e colaboradores(6) analisaram 16 estudos publicados até 2015, alguns deles comparativos com dois grupos paralelos de TAVI com e sem VAB prévia, e outros de um só braço (TAVI sem VAB prévia). Em total, foram 1.395 pacientes: 674 com e 721 sem VAB pré-implante; 793 com válvulas expansíveis por balão (Edwards Sapien e Sapien 3) e 602 com válvulas autoexpansíveis (CoreValve). Na metanálise comparativa, não foram encontradas diferenças em termos de mortalidade (risco relativo [RR] 0,61, 95% CI 0,32-1,14; p = 0,12), desfecho combinado de segurança (morte/AVC/sangramento maior/insuficiência renal aguda/oclusão coronariana/complicação vascular maior) (RR 0,85, 95% CI 0,62-1,18; p = 0,34), insuficiência aórtica moderada a severa (RR 0,68, 95% CI 0,23-1,99; p = 0,48), necessidade de pós-dilatação (RR 0,86, 95% CI 0,66-1,13; p = 0,58), AVC (RR 0,72, 95% CI 0,30-1,71; p = 0,45), e implante de marca-passos (RR 0,80, 95% CI 0,49-1,30; p = 0,37).
No segundo e mais recente estudo, Singh e colaboradores(7) analisaram 2.650 pacientes, 1.043 dos quais tinham sido submetidos a TAVI direto e 1.607 a TAVI com VAB prévia, de 9 estudos comparativos com dois grupos paralelos. Assim como o relatado na metanálise prévia, não foram encontradas diferenças significativas em termos de mortalidade em 30 dias (OR 0,96, 95% CI 0,63-1,47; p = 0,86), AVC (OR 0,81, 95% CI 0,34-1,92; p = 0,63) e implante de marca-passos (OR 0,84, 95% CI 0,66-1,05; p = 0,12); mas neste caso foi encontrada uma significativa menor incidência de insuficiência aórtica moderada/severa nos pacientes que foram submetidos a TAVI direto (OR 0,44, 95% CI 0,20-0,96; p = 0,04).
Por último, Bonaros e col.(8) publicaram recentemente o resultado de um registro prospectivo multicêntrico, onde em 300 pacientes (222 com VAB prévia e 78 com TAVI direto), tratados com Edwards Sapien ou Sapien 3, tampouco foram encontradas diferenças nos desfechos de segurança e eficácia, mas sim uma significativa menor incidência de implante de marca-passos no grupo TAVI direto: 0% vs. 5,0%; p = 0,034.
_
Interpretação
É importante destacar que embora na maioria dos estudos individuais e também nas duas revisões mencionadas não tenham sido registradas diferenças significativas em um grande número de desfechos clinicamente relevantes, também se observa uma tendência a um menor número de eventos na estratégia TAVI direta, tal como pode ser observado nos pontos de estimação de RR e OR sistematicamente menores à unidade (ainda que com amplos intervalos de confiança) em quase todas as comparações.
No caso da ocorrência de insuficiência aórtica moderada a severa, a diferença a favor do TAVI direto alcançou significância estatística em ao menos um estudo individual(9), assim como na revisão citada. É interessante especular acerca das razões deste achado, talvez relacionado com a menor disrupção da valva nativa no implante direto da prótese.
A menor incidência de implante de marca-passos em TAVI direto no registro prospectivo citado(8) e na tendência observada em outros estudos pode ser explicada pelo já conhecido efeito da VAB no sistema de condução(5).
Ao contrário, não foi possível observar diferença significativa ou tendência clara a favor do TAVI direto no que se refere à ocorrência de AVC. Medidos por monitoramento Doppler transcraniano, os eventos embólicos ocorrem em cada etapa do procedimento, especialmente durante o posicionamento da prótese(10), fato que enfatiza a necessidade de uma cuidadosa manipulação do sistema em todas as etapas, e potencialmente a utilização de dispositivos de proteção.
_
Tomada de decisões no paciente individual
Baseando-nos na informação disponível até o momento, não há razão para sustentar o uso sistemático de VAB previamente ao implante. Ao contrário, evitar a pré-dilatação com balão poderia contribuir para reduzir complicações como transtornos de condução e implante de marca-passos ou insuficiência aórtica significativa quando se aplica à população adequada.
Pacientes com calcificação severa ou assimétrica, com áreas menores que 0,5%, estão entre a população que necessitou pré-dilatação em “bail-out” em estudos de TAVI direto(10), e junto aos pacientes com raízes pequenas e escassa distância aos óstios coronarianos naqueles pacientes nos quais é necessário constatar o comportamento das valvas durante a insuflação do balão, são candidatos a requerer a VAB prévia.
A utilização de ecocardiografia transesofágica durante o procedimento poderia contribuir para identificar estes pacientes, com base na análise do anel, da raiz aórtica, do grau de calcificação e da insuficiência e severidade da estenose(11).
_
Tendência atual e futuro
À medida que a indicação de TAVI se estende a populações de menor risco, reduzir a frequência de eventos adversos adquire especial relevância. Evitar a VAB com este objetivo é possível graças à maior experiência e à possibilidade de identificar os pacientes ideais, e isso já pode ser entendido dos últimos registros e dos desenhos dos novos estudos: a frequência de TAVI direto aumentou de 8% a 18% entre 2013 e 2015 no registro italiano(12), e é de se esperar que esta tendência continue.
Por outro lado, também é de se esperar que avanços tecnológicos melhorem os resultados da VAB(fig. 1-2), reduzindo as complicações nos pacientes que a requeiram, com áreas valvulares críticas, severa calcificação e necessidade de avaliação da perviedade coronariana.
A publicação de registros multicêntricos em curso, assim como o desenvolvimento de estudos randomizados a maior escala, serão necessários no futuro para ajudar na tomada de decisões em um contexto de permanente progresso tecnológico.
Figura 1. Balão de perfusão para valvoplastia aórtica TrueFlow (BARD)
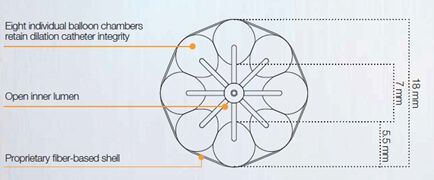
Figura 2. Preservação de fluxo anterógrado durante a valvoplastia aórtica om balão de perfusão.
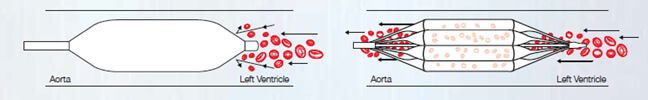
_
Referências Bibliográficas
1.- Grube E, Naber C, Abizaid A, Sousa E, Mendiz O, Lemos P, Kalil Filho R, Mangione J, Buellesfeld L. Feasibility of transcatheter aortic valve implantation without balloon pre-dilation: a pilot study. JACC Cardiovasc Interv. 2011;4:751–757.
2.- Wendler O, Dworakowski R, Monaghan M, MacCarthy PA. Direct transapical aortic valve implantation: a modified transcatheter approach avoiding balloon predilatation. Eur J Cardiothorac Surg. 2012;42:734–736.
3.- Eltchaninoff H, Durand E, Borz B, Furuta A, Bejar K, Canville A, Farhat A, Fraccaro C, Godin M, Tron C, Sakhuja R, Cribier A. Balloon aortic valvuloplasty in the era of transcatheter aortic valve replacement: acute and long-term outcomes. Am Heart J. 2014;167:235–240.
4.- Kumar A, Paniagua D, Hira RS, Alam M, Denktas AE, Jneid H. Balloon aortic valvuloplasty in the transcatheter aortic valve replacement era. J Invasive Cardiol. 2016;28:341–348.
5.- Campelo-Parada F, Nombela-Franco L, Urena M, Regueiro A, Jiménez-Quevedo P, Del Trigo M, Chamandi C, Rodríguez-Gabella T, Auffret V, Abdul-Jawad Altisent O, DeLarochellière R, Paradis JM, Dumont E, Philippon F, Pérez-Castellano N, Puri R, Macaya C, Rodés-Cabau J. Timing of Onset and Outcome of New Conduction Abnormalities Following Transcatheter Aortic Valve Implantation: Role of Balloon Aortic Valvuloplasty. Rev Esp Cardiol (Engl Ed). 2017 May 27.
6.- Bagur R, Kwok CS, Nombela-Franco L, Ludman PF, de Belder MA, Sponga S, Gunning M, Nolan J, Diamantouros P, Teefy PJ, Kiaii B, Chu MW, Mamas MA. Transcatheter aortic valve implantation with or without preimplantation balloon aortic valvuloplasty: a systematic review and meta-analysis. J Am Heart Assoc. 2016;5:e003191. DOI: 10.1161/JAHA.115.003191.
7.- Kuljit Singh, Kristin Carson, Onn Akbar Ali, Rohan Jayasinghe, Alexander Dick, Christopher Glover, Marino Labinaz. Efficacy and Complications of Transcatheter Aortic Valve Implantation With and Without Balloon Aortic Valvuloplasty. J Heart Valve Dis. 2017 Mar;26(2):139-145.
8.- Bonaros N, Kofler M, Frank D, Cocchieri R, Jagielak D, Aiello M, Lapeze J, Laine M, Chocron S, Muir D, Eichinger W, Thielmann M, Labrousse L, Bapat V, Rein KA, Verhoye JP, Gerosa G, Baumbach H, Deutsch C, Bramlage P, Thoenes M, Romano M. Balloon-expandable transaortic transcatheter aortic valve implantation with or without predilation. J Thorac Cardiovasc Surg. 2017 Nov 2.
9.- Fiorina C, Maffeo D, Curello S, Lipartiti F, Chizzola G, D’Aloia A, Adamo M, Mastropierro R, Gavazzi E, Ciccarese C, Chiari E, Ettori F. Direct transcatheter aortic valve implantation with self-expandable bioprosthesis: feasibility and safety. Cardiovasc Revasc Med. 2014;15:200–203.
10.- Kim WK, Praz F, Blumenstein J, Liebetrau C, Gaede L, Van Linden A, Hamm C, Walther T, Windecker S, Mollmann H. Transfemoral aortic valve implantation of Edwards SAPIEN 3 without predilatation. Catheter Cardiovasc Interv.2017;89:E38–E43.
11.- Usefulness of Echocardiographic Criteria for Transcatheter Aortic Valve Implantation without Balloon Predilation: A Single-Center Experience. Islas, Fabián et al. Journal of the American Society of Echocardiography , Volume 28 , Issue 4 , 423 – 429.
12.- Giordano A, Corcione N, Biondi-Zoccai G, Berti S, Petronio AS, Pierli C, Presbitero P, Giudice P, Sardella G, Bartorelli AL, Bonmassari R, Indolfi C, Marchese A, Brscic E, Cremonesi A, Testa L, Brambilla N, Bedogni F. Patterns and trends of transcatheter aortic valve implantation in Italy: insights from RISPEVA. J Cardiovasc Med. 2017;18:96–102



