Durabilidad de la válvula aórtica transcatéter
Durabilidad de la válvula aórtica transcatéter
A. Definición de durabilidad de la válvula bioprotésica
Cuando hablamos de durabilidad en TAVI, tenemos que tomar en cuenta varios aspectos. No solo hablamos de un concepto de tiempo, sino hablamos de los cambios hemodinámicos propios del TAVI y sobre todo los cambios hemodinámicos secundarios al deterioro estructural de la válvula1. Simultáneamente, tenemos que evaluar la presencia de síntomas asociados y la incidencia de eventos clínicos relacionados2.
Todas las guías y consensos de expertos se han tomado la tarea de perfeccionar las definiciones de disfunción de la válvula bioprotésica1-6, que no es lo mismo que la durabilidad. Para esto, una propuesta de definición de durabilidad de la válvula bioprotésica sería la capacidad de la válvula para mantener su integridad estructural y función hemodinámica durante un período prolongado, que idealmente se espera que sea de al menos 10 a 15 años.
Para poder evaluar los diferentes componentes de la definición de durabilidad de la válvula bioprotésica, se deben evaluar diferentes aspectos. Cuando evaluamos la estructura de la válvula, lo hacemos a través de métodos de imagen, típicamente mediante un ecocardiograma transtorácico (ETT)2, y muchas veces se debe complementar con otros métodos como la tomografía computada (TC). Cuando evaluamos su comportamiento hemodinámico, lo hacemos de la misma manera mediante un ETT y complementamos ya sea con un ecocardiograma transesofágico (ETE) y una CT. Cuando evaluamos la durabilidad, lo hacemos en años, y para esto nos basamos en la información proveniente de estudios observacionales y ensayos clínicos con seguimientos a largo plazo. Estos estudios, implementando las definiciones de diferentes consensos y guías 1, reportan la incidencia de diferentes desenlaces, incluidos los diferentes tipos de disfunción de la válvula bioprotésica (estructural, no-estructural, por trombosis o por endocarditis) y la incidencia de falla de la válvula bioprotésica (eventos clínicos relacionados, tales como síntomas, falla cardiaca, muerte o re-intervención). Es a partir del tiempo al evento (tipo de disfunción o falla) donde estos estudios proveen información para estimar la durabilidad en tiempo de estas bioprótesis.
B. Evidencia científica de durabilidad de las bioprótesis BEV y SEV
La cantidad de información con respecto a la durabilidad de la TAVI es vasta y puede ser organizada en dos grandes grupos de acuerdo con la calidad de información que nos pueden brindar: la información proveniente de estudios observacionales (en general registros) y de ensayos clínicos. (Tabla 1)
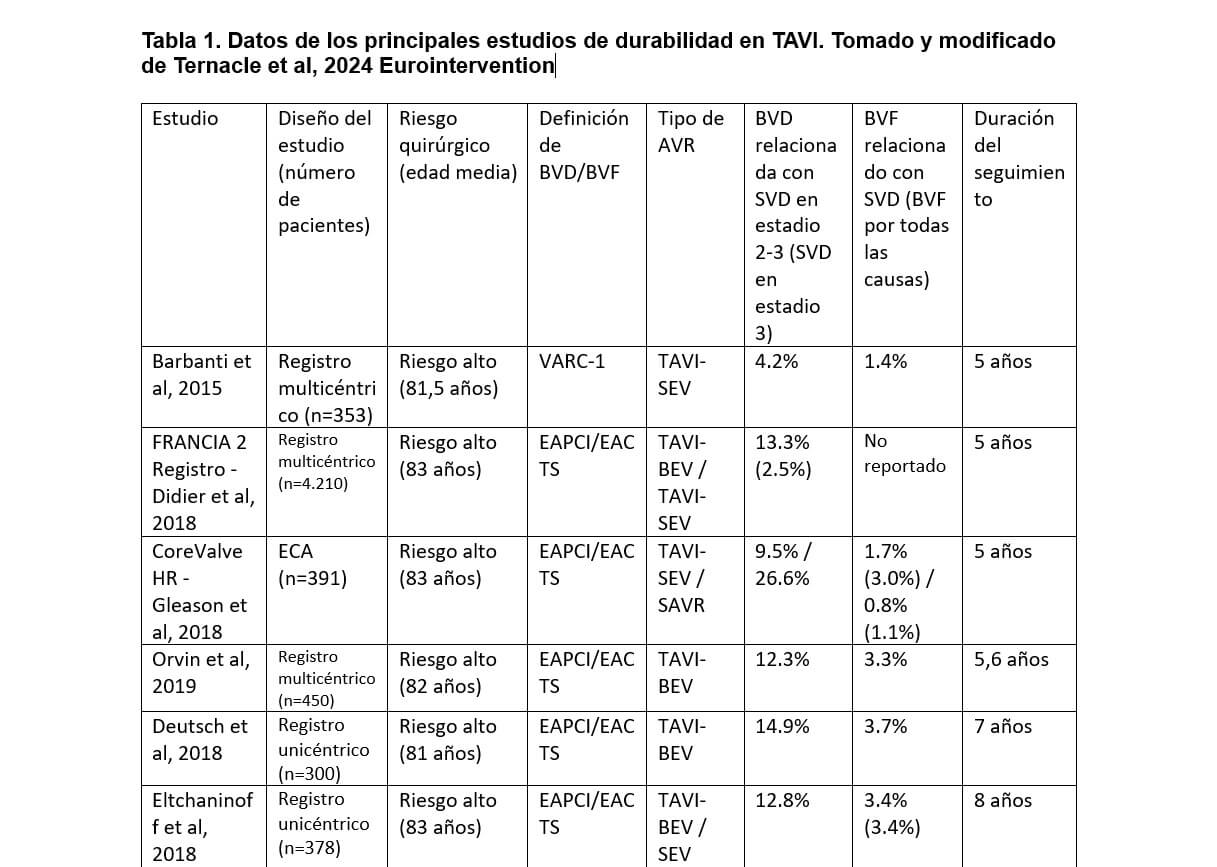
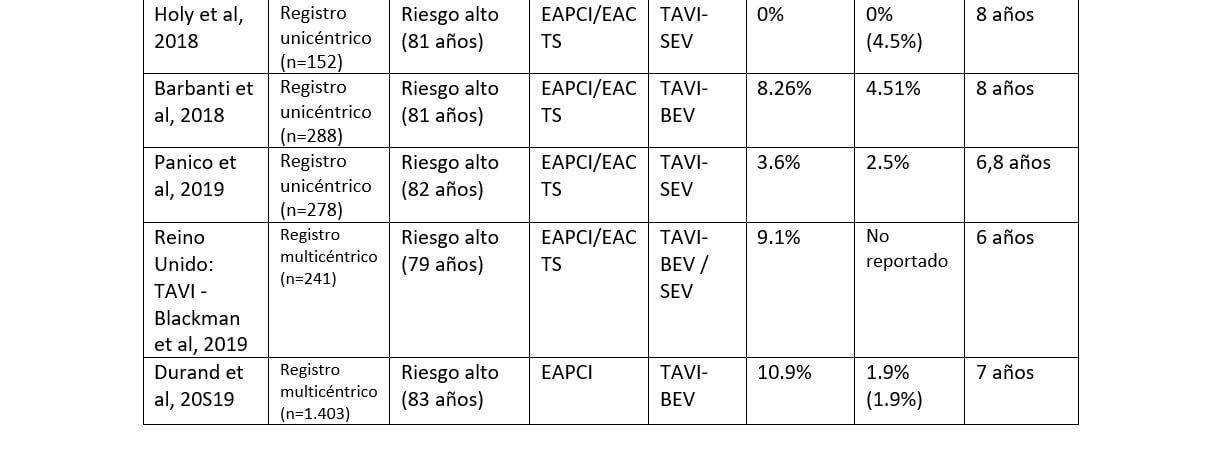
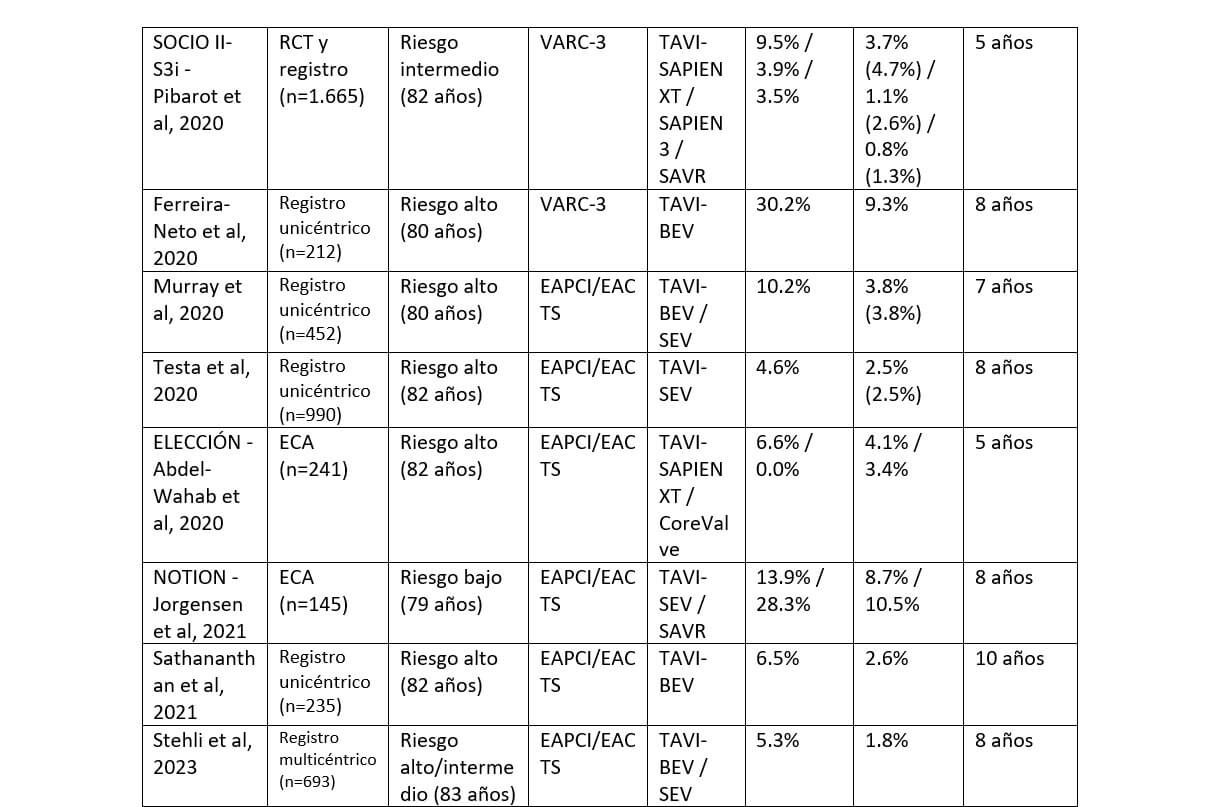
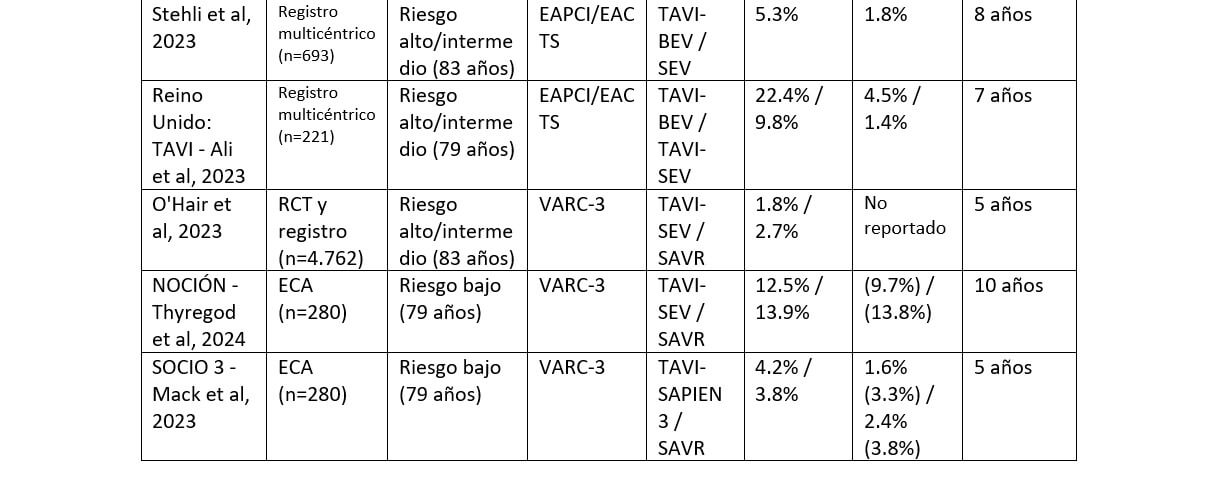
También podemos dividirla cronológicamente en evidencia de durabilidad a corto plazo (menos de 5 años), a mediano plazo (5 a 10 años) y evidencia de durabilidad a largo plazo, cuando hablamos de estudios con seguimiento de 10 años o más. Sin embargo, hay que tener en cuenta que el primer TAVI estuvo disponible recién en 2002 y se trató principalmente a pacientes de edad avanzada o de alto riesgo de muerte no relacionada con las válvulas, es por esto por lo que, los datos sobre la durabilidad ≥5 años aún son limitados.
Los estudios actualmente disponibles sobre la durabilidad a medio plazo de los dispositivos autoexpandibles (self-expandable valve – SEV) se refieren a CoreValve®/Evolut R® (Medtronic), válvulas de pericardio porcino supra anular montado sobre un frame de nitinol, mientras que los estudios sobre dispositivos expandibles con balón (balloon-expandable valve – BEV) se refieren principalmente a pacientes tratados con dispositivos Sapien®/Sapien XT® (Edwards Lifescience) caracterizados por valvas de pericardio bovino montadas sobre un frame de cromo-cobalto. Diferentes iteraciones de diseño y mecanismos de implementación de las válvulas SEV y BEV pueden traducirse en una variación significativa en la durabilidad del dispositivo. De hecho, la posición de las valvas supra anulares de los dispositivos SEV permite teóricamente un área de orificio más alta y, en consecuencia, gradientes más bajos. Por el contrario, los dispositivos BEV, con su mecanismo de sellado mejorado, suelen tener una tasa más baja de fuga paravalvular al precio de gradientes transvalvulares más altos. Los estudios publicados sobre el rendimiento a largo plazo de las válvulas SEV y BEV pueden sugerir que la hemodinámica del flujo directo podría afectar la durabilidad más que las fugas paravalvulares.
Las nuevas iteraciones la familia Sapien actualmente cuenta con un tratamiento al pericardio de sus valvas (RESILIA®) dedicado expresamente como tratamiento anti-calcificación con el objetivo principal de retardar la degeneración estructural y consecuentemente incrementar la durabilidad. Esta iteración de la válvula (Sapien S3 Ultra RESILIA®) es la más actual y tomará 8-10 años conocer los verdaderos resultados de su durabilidad a largo plazo.
Evidencia actual, a 5 años, SEV.
Dos ensayos aleatorios han comparado la durabilidad a medio plazo de CoreValve® y recambio valvular aórtico por cirugía (surgical aortic valve replacement – SAVR): los ensayos clínicos aleatorizados CoreValve US High Risk Pivotal7 y el estudio SURTAVI8. Recientemente se publicó un análisis post hoc donde se combinaron datos de estos dos ensayos clínicos aleatorizados CoreValve US High Risk Pivotal (n = 615) y SURTAVI (n = 1484) y que se complementó con datos del ensayo CoreValve Extreme Risk (n = 485) y del estudio de acceso continuo CoreValve (n = 2178). En este análisis se incluyeron pacientes con estenosis valvular aórtica grave que se consideraba que tenían un riesgo de mortalidad quirúrgica intermedio o mayor a los 30 días. Los pacientes fueron aleatorizados a TAVI SEV o SAVR en los ensayos clínicos o se sometieron a TAVI SEV por indicaciones clínicas en los estudios no aleatorios. En 4,762 pacientes incluidos, la incidencia acumulada de degeneración estructural valvular al tratar la muerte como un riesgo competitivo fue menor en pacientes sometidos a TAVI que a cirugía (TAVI, 2.20 %; cirugía, 4.38 %; índice de riesgo [HR], 0.46; IC del 95%, 0.27-0.78; p=0.004). Este menor riesgo fue más pronunciado en pacientes con anillos más pequeños (23 mm de diámetro o menos; TAVI, 1.32 %; SAVR, 5.84 %; HR, 0.21; IC del 95%, 0.06-0.73; p=0.02). La degeneración estructural valvular se asoció con un aumento de la mortalidad por todas las causas a 5 años (HR, 2.03; IC del 95%, 1.46-2.82; p-0.001), a mortalidad cardiovascular (HR, 1.86; IC del 95%, 1.20-2.90; p=0.006) y hospitalizaciones por enfermedad valvular o empeoramiento de la insuficiencia cardíaca (HR, 2.17; IC del 95%, 1.23-3.84; p=0.008). En resumen, este estudio encontró una menor tasa de degeneración estructural valvular en pacientes sometidos a TAVI SEV vs a SAVR a los 5 años9. (Figura 1)
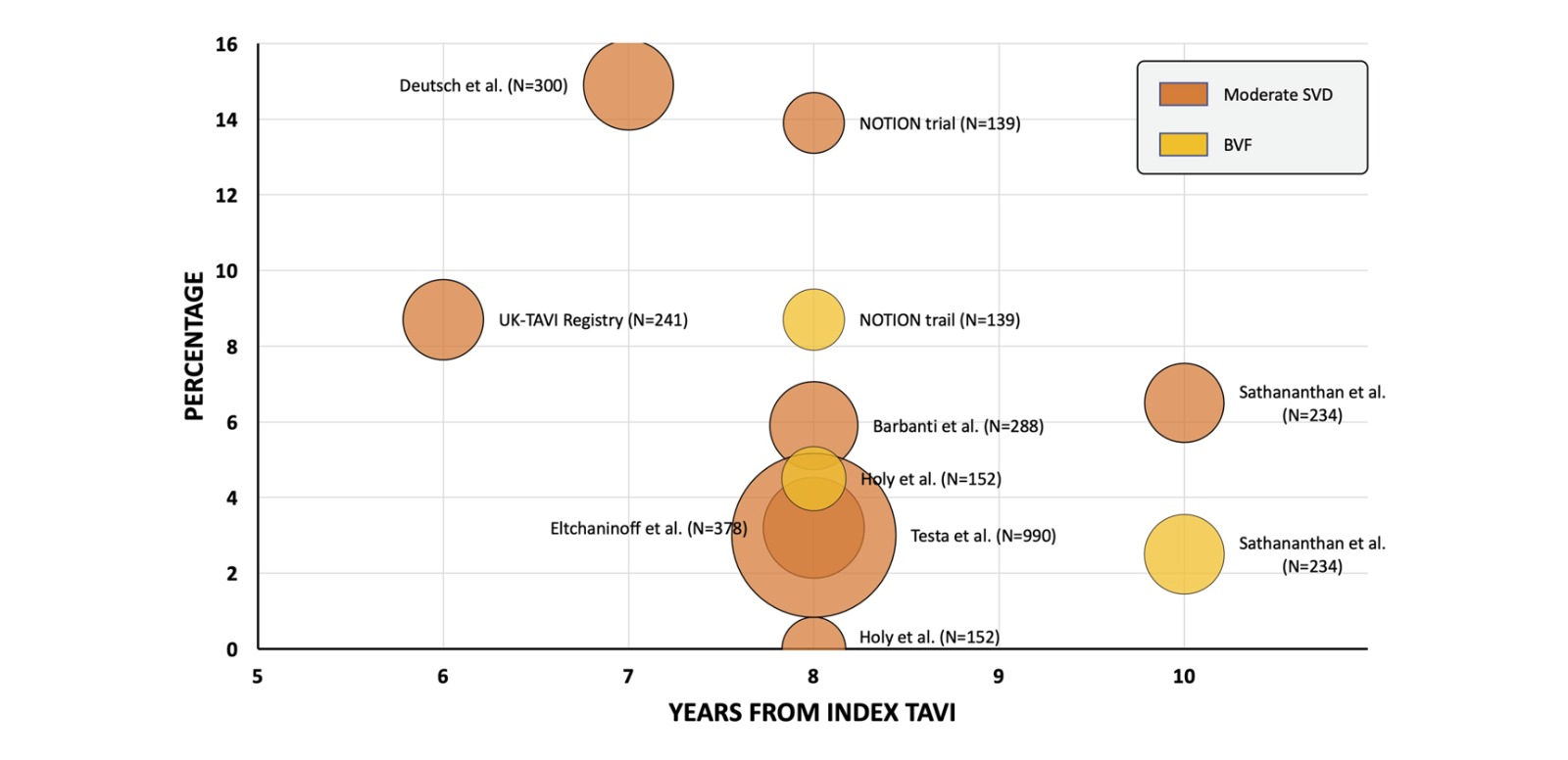
Figura 1. Durabilidad del TAVI a más de 5 años, estudios representativos.
TAVI libre de datos de deterioro estructural moderado y falla de la válvula bioprotésica, más de 5 años. Naranja = deterioro estructural moderado de la válvula; amarillo = falla de la válvula bioprotésica. Gráfico de burbujas representativo del tamaño de la cohorte del estudio. TAVI: implante valvular aórtico transcatéter; SVD = deterioro estructural de la válvula; BVF = fallo de la válvula bioprotésica.
Tomado de: Montarello NJ, Willemen Y, Tirado-Conte G, Travieso A, Bieliauskas G, Sondergaard L, De Backer O. Transcatheter aortic valve durability: a contemporary clinical review. Front Cardiovasc Med. 2023 May 9;10:1195397. doi: 10.3389/fcvm.2023.1195397. PMID: 37229228; PMCID: PMC10203628.
Evidencia actual, a 5 años, BEV
Los estudios PARTNER 110 y PARTNER 1A11 no mostraron casos de degeneración estructural valvular en ambos grupos a los 5 años y un análisis de evaluación longitudinal del ensayo PARTNER I demostró que el rendimiento de la válvula y la hemodinámica cardíaca fueron estables después de la implantación tanto en BEV TAVI como en SAVR en pacientes vivos a los 5 años12. En el ensayo PARTNER 2A, los pacientes fueron asignados aleatoriamente para recibir TAVI con Sapien XT® o SAVR, mientras que, en el registro SAPIEN 3, los pacientes fueron asignados a TAVI con Sapien 3®. En comparación con SAVR, la cohorte Sapien XT® TAVI tuvo una tasa de incidencia ajustadas por exposición a 5 años significativamente más altas (por 100 pacientes-año) de degeneración estructural valvular (1.61 ± 0.24% frente a 0.63 ± 0.16%) y falla de la válvula relacionada con degeneración estructural valvular (0.58 ± 0.14% frente a 0.12 ± 0.07%). Las tasas a 5 años de degeneración estructural valvular según VARC 3, falla de la válvula relacionada con degeneración estructural valvular y falla de la válvula por todas las causas en Sapien 3® TAVI no fueron significativamente diferentes de la cohorte SAVR. (Figura 1). En comparación con SAVR, la válvula de balón expandible SAPIEN XT de segunda generación tuvo una tasa más alta de SVD a 5 años, mientras que la SAPIEN 3 de tercera generación tiene una tasa de SVD que no fue diferente de la SAVR13. (Figura 1)
Recientemente, los resultados a cinco años del estudio Evolut Low Risk respaldan la durabilidad y eficacia hemodinámica de la válvula transcatéter Evolut™ en pacientes de bajo riesgo. El estudio SMART en pequeños anillos demuestra que las válvulas autoexpandibles Evolut presentan menor disfunción valvular que las balón expandibles Sapien 3, con un rendimiento valvular superior a 2 años de seguimiento clínico, sin diferencias en eventos clínicos.(13 Bis) El seguimiento a cinco años del ensayo SMART brindará mayor comprensión sobre si estas ventajas hemodinámicas se traducen en una mayor durabilidad de la válvula y mejores resultados para los pacientes.
Evidencia actual, a 5 años, SEV vs BEV
El ensayo CHOICE aleatorizó a 241 pacientes de alto riesgo a TAVI con dispositivo BEV o SEV. A los 5 años de seguimiento, la degeneración estructural valvular moderada/grave fue poco común pero significativamente mayor en pacientes que recibieron un BEV en comparación con aquellos que recibieron un SEV (6.6% vs 0%, p=0.018)14.
Los datos más grandes del registro de durabilidad TAV bioprotésica a medio plazo de 5 años se obtienen del registro FRANCE-215. Este registro incluyó a 4,201 pacientes sometidos a TAVI con TAV SEV (32 %) vs BEV (68%) y demostró una tasa de degeneración estructural valvular moderada y grave del 8.9% y 0% para el dispositivo SEV, y del 13.8 % y 4.1 % para los BEV TAVI. Sin embargo, la aparición de degeneración estructural valvular grave no se correlacionó con un exceso de mortalidad, posiblemente debido al hecho de que la mayoría de los casos graves de degeneración estructural valvular se definieron por un gradiente medio aumentado en lugar de insuficiencia aórtica grave.
Evidencia actual, mediano plazo, > 5 años.
El registro U.K. TAVI16 evaluó la incidencia de degeneración estructural valvular en 241 pacientes tratados con dispositivos SEV (66%) y BEV (34%). El seguimiento varió de 5 a 10 años (mediana de seguimiento 5.8 años). En este estudio no se encontraron diferencias en las tasas de degeneración estructural valvular moderada entre tipos de válvulas, el 91% de los pacientes estuvo libre de degeneración estructural valvular mientras que el único caso informado de degeneración estructural valvular grave fue en el grupo SEV17. Holy et al. informaron resultados a largo plazo de 152 pacientes sucesivos que habían sido sometidos a TAVI con CoreValve® entre 2007 y 2011. El seguimiento ecocardiográfico se realizó a los 6.3 +/- 1.0 años en el 88% de los pacientes que sobrevivieron más de 5 años. No se registró ningún caso de deterioro estructural valvular y 5 pacientes (3.3%) habían sido sometidos a redo-TAVI o cirugía por fuga paravalvular18.
Durand et al analizaron pacientes consecutivos con al menos 5 años de seguimiento disponibles sometidos a TAVI en 5 centros franceses. Incluyeron 1403 pacientes y usaron BEV en el 83.7% de los casos. La falla de la válvula bioprotésica ocurrió en 19 pacientes con una incidencia acumulada a 7 años del 1.9% (IC del 95%, 1.4%-2.4%). El deterioro estructural de la válvula se produjo en 49 pacientes (moderada, n=32; grave, n=17) con una incidencia acumulada de 7 años de deterioro estructural de la válvula moderado o grave del 7.0% (IC del 95%, 5.6 %-8.4 %) y del 4.2% (IC del 95%, 2.9%-5.5%), respectivamente. Las incidencias de SVD y falla de la válvula bioprotésica no fueron significativamente diferentes entre las prótesis con balón y las autoexpandibles19.
Deutsch et al. Publicaron los resultados de un registro prospectivo unicéntrico de pacientes sometidos a TAVI con dispositivos de primera generación (n=214 CoreValve; n=86 SAPIEN). A los siete años, la incidencia acumulada bruta general de deterioro estructural de la válvula según la definición de EAPCI/ESC/EACTS de 2017 fue del 14.9 % (CoreValve® 11.8 % frente a SAPIEN® 22.6 %; p=0.01). Es importante señalar que tras 7 años después del TAVI, solo el 23.2% de los pacientes de alto riesgo seguían vivos20.
Barbanti et al.21 de un total de 288 pacientes tratados con CoreValve® (82.3%) o Sapien XT® (16.7%), encontraron una función de incidencia acumulada de 8 años de degeneración estructural valvular moderada y grave de, respectivamente, 5.87% y 2.39%.
Elchaninoff et al. mostró en 378 pacientes tratados con BEV una incidencia de degeneración estructural valvular a 8 años del 3.4%22. Testa et al. informaron sobre 990 pacientes sometidos a TAVI con CoreValve®/Evolut-R® y documentaron una incidencia acumulada en 8 años de deterioro estructural valvular moderado y deterioro estructural valvular grave del 3.0% y el 1.6%, respectivamente23.
Evidencia actual, largo plazo, > 10 años
Sathananthan et al.24 en 235 pacientes consecutivos tratados con Cribier-Edwards® (20.9%), Edwards SAPIEN® (77.4%) o CoreValve® (1.7%), informaron una incidencia acumulada de 10 años de degeneración estructural valvular del 6.5%.
Scotti25 analizaron un total de 604 pacientes del registro PUREVALVE sometidos a TAVI y fueron analizados según la altura del nuevo plano valvular en intra anular (IA) (Sapien/-XT/-3® y Lotus®, n=482) y supra anular (SA) (CoreValve/Evolut R® y Acurate®, n=122. En comparación con la TAVI SA, los gradientes transaórticos medios fueron significativamente mayores y aumentaron con el tiempo en el grupo IA. Las TAVI IA mostraron mayores incidencias acumuladas a 10 años de fallo (IA 8% vs. SA 1%, p = 0.02) y degeneración estructural grave (IA 5% vs. SA 1%, p = 0.05), principalmente en los dispositivos TAVR más pequeños (20-23 mm). Después de excluir estos tamaños, las incidencias acumuladas de BVF (IA 5% vs. SA 1%, p=0.40) y HVD grave (IA 2% vs. SA 1%, p=0.11) fueron similares.
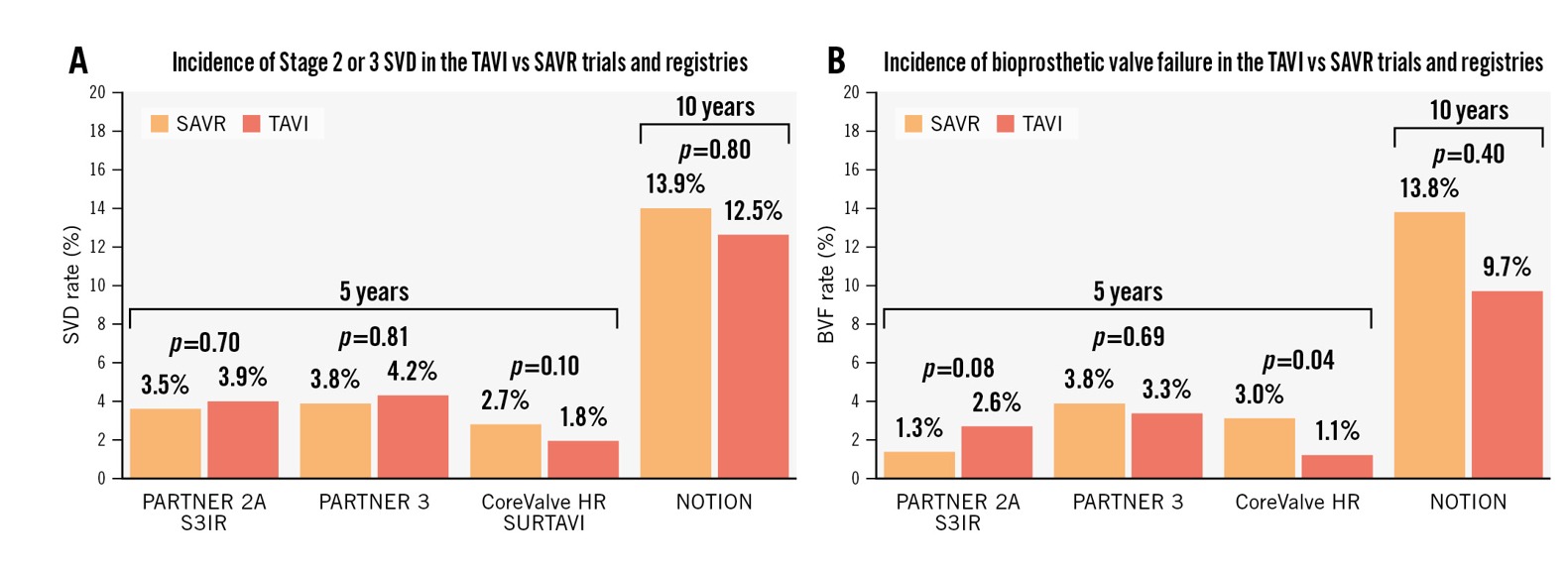
Por último, el ensayo NOTION enroló a 280 pacientes de bajo riesgo aleatorizados 1:1 a TAVI con CoreValve® o SAVR, recientemente ha publicado los datos de largo plazo de seguimiento a 10 años. Se produjo deterioro estructural grave en el 1.5 % y el 10.0 % (HR 0.2; IC 95% 0.04–0.7; p=0.02) después de TAVI y SAVR, respectivamente. La incidencia acumulada de deterioro no-estructural grave fue del 20.5% y 43.0% (p-0.001) y de endocarditis del 7.2 % y 7.4 % (p=1.0) después de TAVI y SAVR, respectivamente. Ningún paciente tuvo trombosis valvular clínica. La falla de la válvula bioprotésica ocurrió en 9.7% de los pacientes con TAVI y 13.8 % de los pacientes con SAVR (HR 0.7; IC 95% 0.4-1.5; p=0.4)26. (Figura 1 y 2)
Figura 2. Incidencia de SVD en estadio 2 o 3 o de BVF por todas las causas según VARC-3 en los ECA y registros TAVI versus SAVR. Incidencia de SVD (A) en estadio 2 (moderada) o 3 (grave) y de BVF (B) por todas las causas según las definiciones de VARC-3 en el ensayo PARTNER 2A y S3IR, en el ensayo PARTNER 3, en el ensayo CoreValve HR y en el ensayo SURTAVI a los 5 años y en el ensayo NOTION a los 10 años. BVF: fallo valvular bioprotésico; CoreValve HR: Prueba fundamental de Medtronic CoreValve en EE. UU.; ECA: ensayo controlado aleatorizado; SAVR: reemplazo quirúrgico de la válvula aórtica; SVD: deterioro estructural de la válvula; TAVI: implante de válvula aórtica transcatéter; VARC-3: Consorcio de Investigación Académica de Válvulas 3. Tomado y traducido de Ternacle et al, 2024 Eurointervention.
Bibliografía
- Richter I, Thiele H, Abdel-Wahab M. Durability of Transcatheter Heart Valves: Standardized Definitions and Available Data. J Clin Med. 2021;10
- Pibarot P, Herrmann HC, Wu C, Hahn RT, Otto CM, Abbas AE, Chambers J, Dweck MR, Leipsic JA, Simonato M, Rogers T, Sathananthan J, Guerrero M, Ternacle J, Wijeysundera HC, Sondergaard L, Barbanti M, Salaun E, Genereux P, Kaneko T, Landes U, Wood DA, Deeb GM, Sellers SL, Lewis J, Madhavan M, Gillam L, Reardon M, Bleiziffer S, O'Gara PT, Rodes-Cabau J, Grayburn PA, Lancellotti P, Thourani VH, Bax JJ, Mack MJ, Leon MB, Heart Valve C. Standardized Definitions for Bioprosthetic Valve Dysfunction Following Aortic or Mitral Valve Replacement: JACC State-of-the-Art Review. J Am Coll Cardiol. 2022;80:545-561
- Varc-3 Writing C, Genereux P, Piazza N, Alu MC, Nazif T, Hahn RT, Pibarot P, Bax JJ, Leipsic JA, Blanke P, Blackstone EH, Finn MT, Kapadia S, Linke A, Mack MJ, Makkar R, Mehran R, Popma JJ, Reardon M, Rodes-Cabau J, Van Mieghem NM, Webb JG, Cohen DJ, Leon MB. Valve Academic Research Consortium 3: Updated Endpoint Definitions for Aortic Valve Clinical Research. J Am Coll Cardiol. 2021;77:2717-2746
- Capodanno D, Petronio AS, Prendergast B, Eltchaninoff H, Vahanian A, Modine T, Lancellotti P, Sondergaard L, Ludman PF, Tamburino C, Piazza N, Hancock J, Mehilli J, Byrne RA, Baumbach A, Kappetein AP, Windecker S, Bax J, Haude M. Standardized definitions of structural deterioration and valve failure in assessing long-term durability of transcatheter and surgical aortic bioprosthetic valves: a consensus statement from the European Association of Percutaneous Cardiovascular Interventions (EAPCI) endorsed by the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur J Cardiothorac Surg. 2017;52:408-417
- Otto CM, Nishimura RA, Bonow RO, Carabello BA, Erwin JP, Gentile F, Jneid H, Krieger EV, Mack M, McLeod C, O’Gara PT, Rigolin VH, Sundt TM, Thompson A, Toly C. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2021;143:e72-e227
- Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J, Capodanno D, Conradi L, De Bonis M, De Paulis R, Delgado V, Freemantle N, Gilard M, Haugaa KH, Jeppsson A, Juni P, Pierard L, Prendergast BD, Sadaba JR, Tribouilloy C, Wojakowski W, Group EESD. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022;43:561-632
- Gleason TG, Reardon MJ, Popma JJ, Deeb GM, Yakubov SJ, Lee JS, Kleiman NS, Chetcuti S, Hermiller JB, Jr., Heiser J, Merhi W, Zorn GL, 3rd, Tadros P, Robinson N, Petrossian G, Hughes GC, Harrison JK, Conte JV, Mumtaz M, Oh JK, Huang J, Adams DH. 5-Year Outcomes of Self-Expanding Transcatheter Versus Surgical Aortic Valve Replacement in High-Risk Patients. J Am Coll Cardiol. 2018;72:2687-2696
- Van Mieghem NM, Deeb GM, Søndergaard L, Grube E, Windecker S, Gada H, Mumtaz M, Olsen PS, Heiser JC, Merhi W, Kleiman NS, Chetcuti SJ, Gleason TG, Lee JS, Cheng W, Makkar RR, Crestanello J, George B, George I, Kodali S, Yakubov SJ, Serruys PW, Lange R, Piazza N, Williams MR, Oh JK, Adams DH, Li S, Reardon MJ. Self-expanding Transcatheter vs Surgical Aortic Valve Replacement in Intermediate-Risk Patients: 5-Year Outcomes of the SURTAVI Randomized Clinical Trial. JAMA Cardiol. 2022;7:1000-1008
- O'Hair D, Yakubov SJ, Grubb KJ, Oh JK, Ito S, Deeb GM, Van Mieghem NM, Adams DH, Bajwa T, Kleiman NS, Chetcuti S, Søndergaard L, Gada H, Mumtaz M, Heiser J, Merhi WM, Petrossian G, Robinson N, Tang GHL, Rovin JD, Little SH, Jain R, Verdoliva S, Hanson T, Li S, Popma JJ, Reardon MJ. Structural Valve Deterioration After Self-Expanding Transcatheter or Surgical Aortic Valve Implantation in Patients at Intermediate or High Risk. JAMA Cardiol. 2023;8:111-119
- Kapadia SR, Leon MB, Makkar RR, Tuzcu EM, Svensson LG, Kodali S, Webb JG, Mack MJ, Douglas PS, Thourani VH, Babaliaros VC, Herrmann HC, Szeto WY, Pichard AD, Williams MR, Fontana GP, Miller DC, Anderson WN, Akin JJ, Davidson MJ, Smith CR. 5-year outcomes of transcatheter aortic valve replacement compared with standard treatment for patients with inoperable aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet. 2015;385:2485-2491
- Mack MJ, Leon MB, Smith CR, Miller DC, Moses JW, Tuzcu EM, Webb JG, Douglas PS, Anderson WN, Blackstone EH, Kodali SK, Makkar RR, Fontana GP, Kapadia S, Bavaria J, Hahn RT, Thourani VH, Babaliaros V, Pichard A, Herrmann HC, Brown DL, Williams M, Akin J, Davidson MJ, Svensson LG. 5-year outcomes of transcatheter aortic valve replacement or surgical aortic valve replacement for high surgical risk patients with aortic stenosis (PARTNER 1): a randomised controlled trial. Lancet. 2015;385:2477-2484
- Daubert MA, Weissman NJ, Hahn RT, Pibarot P, Parvataneni R, Mack MJ, Svensson LG, Gopal D, Kapadia S, Siegel RJ, Kodali SK, Szeto WY, Makkar R, Leon MB, Douglas PS. Long-Term Valve Performance of TAVR and SAVR: A Report From the PARTNER I Trial. JACC Cardiovasc Imaging. 2016
- Pibarot P, Ternacle J, Jaber WA, Salaun E, Dahou A, Asch FM, Weissman NJ, Rodriguez L, Xu K, Annabi MS, Guzzetti E, Beaudoin J, Bernier M, Leipsic J, Blanke P, Clavel MA, Rogers E, Alu MC, Douglas PS, Makkar R, Miller DC, Kapadia SR, Mack MJ, Webb JG, Kodali SK, Smith CR, Herrmann HC, Thourani VH, Leon MB, Hahn RT. Structural Deterioration of Transcatheter Versus Surgical Aortic Valve Bioprostheses in the PARTNER-2 Trial. J Am Coll Cardiol. 2020;76:1830-1843
13 Bis. N Engl J Med 2024;390:1959-1971 DOI: 10.1056/NEJMoa2312573 SMART trial. - Abdel-Wahab M, Landt M, Neumann FJ, Massberg S, Frerker C, Kurz T, Kaur J, Toelg R, Sachse S, Jochheim D, Schäfer U, El-Mawardy M, Robinson DR, Richardt G. 5-Year Outcomes After TAVR With Balloon-Expandable Versus Self-Expanding Valves: Results From the CHOICE Randomized Clinical Trial. JACC Cardiovasc Interv. 2020;13:1071-1082
- Didier R, Eltchaninoff H, Donzeau-Gouge P, Chevreul K, Fajadet J, Leprince P, Leguerrier A, Lièvre M, Prat A, Teiger E, Lefevre T, Tchetché D, Carrié D, Himbert D, Albat B, Cribier A, Sudre A, Blanchard D, Rioufol G, Collet F, Houel R, Dos Santos P, Meneveau N, Ghostine S, Manigold T, Guyon P, Cuisset T, Le Breton H, Delepine S, Favereau X, Souteyrand G, Ohlmann P, Doisy V, Lognoné T, Gommeaux A, Claudel JP, Bourlon F, Bertrand B, Iung B, Gilard M. Five-Year Clinical Outcome and Valve Durability After Transcatheter Aortic Valve Replacement in High-Risk Patients. Circulation. 2018;138:2597-2607
- Ludman PF. UK TAVI registry. Heart. 2019;105:s2-s5
- Blackman DJ, Saraf S, MacCarthy PA, Myat A, Anderson SG, Malkin CJ, Cunnington MS, Somers K, Brennan P, Manoharan G, Parker J, Aldalati O, Brecker SJ, Dowling C, Hoole SP, Dorman S, Mullen M, Kennon S, Jerrum M, Chandrala P, Roberts DH, Tay J, Doshi SN, Ludman PF, Fairbairn TA, Crowe J, Levy RD, Banning AP, Ruparelia N, Spence MS, Hildick-Smith D. Long-Term Durability of Transcatheter Aortic Valve Prostheses. J Am Coll Cardiol. 2019;73:537-545
- Holy EW, Kebernik J, Abdelghani M, Stämpfli SF, Hellermann J, Allali A, El-Mawardy M, Sachse S, Lüscher TF, Tanner FC, Richardt G, Abdel-Wahab M. Long-term durability and haemodynamic performance of a self-expanding transcatheter heart valve beyond five years after implantation: a prospective observational study applying the standardised definitions of structural deterioration and valve failure. EuroIntervention. 2018;14:e390-e396
- Durand E, Sokoloff A, Urena-Alcazar M, Chevalier B, Chassaing S, Didier R, Tron C, Litzler PY, Bouleti C, Himbert D, Hovasse T, Bar O, Avinée G, Iung B, Blanchard D, Gilard M, Cribier A, Lefevre T, Eltchaninoff H. Assessment of Long-Term Structural Deterioration of Transcatheter Aortic Bioprosthetic Valves Using the New European Definition. Circ Cardiovasc Interv. 2019;12:e007597
- Deutsch MA, Erlebach M, Burri M, Hapfelmeier A, Witt OG, Ziegelmueller JA, Wottke M, Ruge H, Krane M, Piazza N, Bleiziffer S, Lange R. Beyond the five-year horizon: long-term outcome of high-risk and inoperable patients undergoing TAVR with first-generation devices. EuroIntervention. 2018;14:41-49
- Barbanti M, Costa G, Zappulla P, Todaro D, Picci A, Rapisarda G, Di Simone E, Sicuso R, Buccheri S, Gulino S, Pilato G, La Spina K, D'Arrigo P, Valvo R, Indelicato A, Giannazzo D, Immè S, Tamburino C, Patanè M, Sgroi C, Giuffrida A, Trovato D, Monte IP, Deste W, Capranzano P, Capodanno D, Tamburino C. Incidence of Long-Term Structural Valve Dysfunction and Bioprosthetic Valve Failure After Transcatheter Aortic Valve Replacement. J Am Heart Assoc. 2018;7:e008440
- Eltchaninoff H, Durand E, Avinée G, Tron C, Litzler PY, Bauer F, Dacher JN, Werhlin C, Bouhzam N, Bettinger N, Candolfi P, Cribier A. Assessment of structural valve deterioration of transcatheter aortic bioprosthetic balloon-expandable valves using the new European consensus definition. EuroIntervention. 2018;14:e264-e271
- Testa L, Latib A, Brambilla N, De Marco F, Fiorina C, Adamo M, Giannini C, Angelillis M, Barbanti M, Sgroi C, Poli A, Ferrara E, Bruschi G, Russo CF, Matteo M, De Felice F, Musto C, Curello S, Colombo A, Tamburino C, Petronio AS, Bedogni F. Long-term clinical outcome and performance of transcatheter aortic valve replacement with a self-expandable bioprosthesis. Eur Heart J. 2020;41:1876-1886
- Sathananthan J, Lauck S, Polderman J, Yu M, Stephenson A, Sathananthan G, Moss R, Cheung A, Ye J, Blanke P, Leipsic J, Wood DA, Webb JG. Ten year follow-up of high-risk patients treated during the early experience with transcatheter aortic valve replacement. Catheter Cardiovasc Interv. 2021;97:E431-e437
- Scotti A, Fovino LN, Coisne A, Fabris T, Cardaioli F, Massussi M, Rodinò G, Barolo A, Boiago M, Continisio S, Montonati C, Sciarretta T, Zuccarelli V, Bernardini V, Masiero G, Napodano M, Fraccaro C, Marchese A, Esposito G, Granada JF, Latib A, Iliceto S, Tarantini G. 10-Year Impact of Transcatheter Aortic Valve Replacement Leaflet Design (Intra- Versus Supra-Annular) in Mortality and Hemodynamic Performance. Front Cardiovasc Med. 2022;9:924958
- Thyregod HGH, Jørgensen TH, Ihlemann N, Steinbrüchel DA, Nissen H, Kjeldsen BJ, Petursson P, De Backer O, Olsen PS, Søndergaard L. Transcatheter or surgical aortic valve implantation: 10-year outcomes of the NOTION trial. Eur Heart J. 2024;45:1116-1124



