Rol de la Valvuloplastia Aórtica en TAVI
Desde que Alain Cribier reportara su primera experiencia con el implante de válvula aórtica por catéter (TAVI), la valvuloplastia aórtica con balón (VAB) se impuso como un paso previo mandatorio para asegurar el pasaje y la expansión de la prótesis en válvulas nativas severamente calcificadas y estenóticas, y a la vez evitar el potencial compromiso hemodinámico durante el posicionamiento.
Esta situación no fue cuestionada inicialmente, en parte debido al alto perfil de los sistemas de primera generación disponibles como la Edwards Sapien (Edwards LifeSience) de 22 y 24 Fr, y la primera CoreValve (Medtronic) de 24 Fr.
El gran desarrollo tecnológico en la primera década permitió la disponibilidad de sistemas más flexibles y de menor perfil. Se comenzó entonces a cuestionar la necesidad de la VAB, apareció la primera experiencia con implante directo (sin VAB previa) con CoreValve de 18(1) Fr y Sapien XT(2) y a reconocerse más claramente la potencial morbilidad asociada a la predilatación.
_
Riesgo/Beneficio de la Valvuloplastia Aórtica con Balón
La VAB está lejos de ser un procedimiento inocuo. Durante más de dos décadas se utilizó como tratamiento paliativo o como puente al reemplazo quirúrgico y esa experiencia muestra una mensurable tasa de complicaciones específicas: muerte 1.5%, accidente cerebro-vascular (ACV) 18%(3), ruptura del anillo 0.3%, insuficiencia aórtica severa 1.1%(4). En estudios comparativos de TAVI con y sin VAB previa, la ocurrencia de nuevo bloqueo de rama izquierda y bloqueo AV completo fue más frecuente a 30 días y más persistente al año cuando se realizó VAB previo al implante (5).
Menos presente en los estudios pero evidente desde la experiencia, la VAB puede ser muy mal tolerada en pacientes con deterioro severo de la función ventricular y/o hipertensión pulmonar.
Por otro lado la VAB brinda información relevante acerca del comportamiento de las valvas en las anatomías con raíz estrecha cuando la distancia desde el anillo a los ostiums coronarios no supera los 12 mm y el riesgo de oclusión es alto. También se ha especulado respecto a la mayor incidencia de post-dilatación (y sus complicaciones específicas asociadas) cuando el implante es directo, sin VAB previa.
_
Estudios comparativos entre TAVI “directo” versus VAB previo
¿Podemos evitar la morbilidad asociada a la VAB implantando directamente la válvula?
Aunque esta cuestión ha suscitado considerable interés, la mayoría de la experiencia proviene de publicaciones de casuísticas de un solo centro, en general con escaso número de pacientes.
Dos recientes revisiones sistemáticas de la literatura aportaron valiosa información en este contexto.
En la primera de ellas, Bagur y colaboradores(6) analizaron 16 estudios publicados hasta 2015, algunos de ellos comparativos con dos grupos paralelos TAVI con y sin VAB previa, y otros de una sola rama (TAVI sin VAB previa). En total 1395 pacientes: 674 con y 721 sin VAB pre implante; 793 con válvulas expandibles con balón (Edwards Sapien y Sapien 3) y 602 con válvulas autoexpandibles (CoreValve). En el meta análisis comparativo, no encontraron diferencias en mortalidad (riesgo relativo [RR] 0.61, 95% CI 0.32– 1.14, P= 0.12), punto final combinado de seguridad (muerte/ACV/sangrado mayor/insuficiencia renal aguda/oclusión coronaria/ complicación vascular mayor) (RR 0.85, 95% CI 0.62– 1.18, P= 0.34), insuficiencia aórtica moderada a severa (RR 0.68, 95% CI 0.23– 1.99, P= 0.48), necesidad de post-dilatación (RR 0.86, 95% CI 0.66– 1.13, P= 0.58), ACV (RR 0.72, 95% CI 0.30– 1.71, P= 0.45), e implante de marcapasos (RR 0.80, 95% CI 0.49– 1.30, P= 0.37).
En el segundo y más reciente estudio, Singh y colaboradores(7) analizaron 2,650 pacientes, 1,043 TAVI directo y 1,607 con VAB previa, de 9 estudios comparativos con dos grupos paralelos. Al igual que en el meta análisis previo, no encontraron diferencias significativas en mortalidad a 30 días (OR 0.96, 95% CI 0.63-1.47, p = 0.86), ACV (OR 0.81, 95% CI 0.34-1.92, p = 0.63) e implante de marcapasos (OR 0.84, 95% CI 0.66- 1.05, p = 0.12); pero en este caso sí encontraron una significativa menor incidencia de insuficiencia aórtica moderara/severa en los pacientes con TAVI directo (OR 0.44, 95% CI 0.20-0.96, p = 0.04).
Por último Bonaros y col. (8), publicaron recientemente el resultado de un registro prospectivo multicéntrico, donde en 300 pacientes (222 con VAB previo y 78 directo), tratados con Sapien Edwards o Sapien 3, tampoco encontraron diferencias en los puntos finales de seguridad y eficacia, pero sí una significativa menor incidencia de implante de marcapasos en el grupo TAVI directo: 0% vs 5.0%; P = .034.
_
Interpretación
Es importante destacar que aunque en la mayoría de los estudios individuales y también en las dos revisiones citadas no hubo diferencias significativas en un importante número de puntos finales clínicamente relevantes, también se observa una tendencia hacia un menor número de eventos en la estrategia TAVI directa, tal como puede observarse en los puntos de estimación de RR y OR sistemáticamente menores a la unidad (aunque con amplios intervalos de confianza) en casi todas las comparaciones.
En el caso de la ocurrencia de insuficiencia aórtica moderada a severa, la diferencia a favor del TAVI directo alcanzó significación estadística en al menos un estudio individual (9), además de en la revisión citada. Resulta interesante especular acerca de las razones de este hallazgo, quizás relacionado a la menor disrupción de la válvula nativa en el implante directo de la prótesis.
La menor incidencia de implante de marcapasos en TAVI directo en el registro prospectivo citado(8), y en la tendencia observada en otros estudios, puede explicarse por el ya conocido efecto de la VAB en el sistema de conducción (5).
En cambio no puede observarse diferencia significativa o tendencia clara a favor del TAVI directo en cuanto a la ocurrencia de ACV. Medidos por monitoreo Doppler trans-craneal, los eventos embólicos ocurren en cada etapa del procedimiento, especialmente durante el posicionamiento de la prótesis(10), lo cual enfatiza la necesidad de una cuidadosa manipulación del sistema en todas las etapas, y potencialmente la utilización de dispositivos de protección.
_
Toma de decisiones en el paciente individual
Basado en la información disponible hasta el momento, no hay razón para sostener el uso sistemático de VAB previo al implante. Por el contrario, evitar la predilatación con balón podría contribuir a reducir complicaciones como trastornos de conducción e implante de marcapasos o insuficiencia aórtica significativa cuando se aplica a la población adecuada.
Pacientes con calcificación severa o asimétrica, con áreas menores a 0.5% están entre la población que necesitó predilatación en “bail-out” en estudios de TAVI directo(10), y junto a los pacientes con raíces pequeñas y escasa distancia a los ostiums coronarios en quienes es necesario constatar el comportamiento de las valvas durante la insuflación del balón, son candidatos a requerir la VAB previa.
La utilización de ecocardiografía transesofágica durante el procedimiento podría contribuir a identificar a estos pacientes, basado en el análisis del anillo, la raíz aórtica, el grado de calcificación e insuficiencia y la severidad de la estenosis(11).
_
Tendencia actual y futuro
A medida que la indicación de TAVI se extiende a poblaciones de menor riesgo, reducir la frecuencia de eventos adversos adquiere especial relevancia. Evitar la VAB con este objetivo, es posible gracias a la mayor experiencia y a la posibilidad de identificar a los pacientes ideales, y esto ya se traduce en los últimos registros y en el diseño de los nuevos estudios: la frecuencia de TAVI directo aumentó del 8% al 18% entre 2013 y 2015 en el registro italiano(12), y es de esperar que esta tendencia continúe.
Por otro lado es de esperar también que avances tecnológicos mejoren los resultados de la VAB(fig. 1-2), reduciendo las complicaciones en los pacientes que la requieran, con áreas valvulares críticas, severa calcificación y necesidad de evaluar la permeabilidad coronaria.
La publicación de registros multicéntricos en curso, y el desarrollo de estudios randomizados a mayor escala, serán necesarios en el futuro para ayudar en la toma de decisiones en un contexto de permanente progreso tecnológico.
Figura 1. Balón de perfusión para valvuloplastia aórtica TrueFlow (BARD)
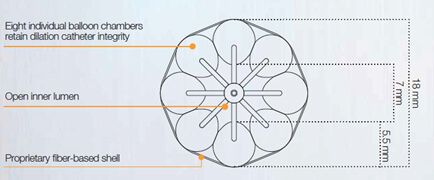
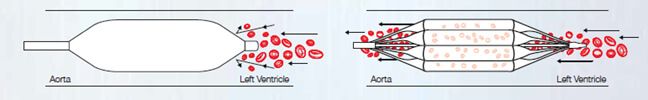
Figura 2. Preservación de flujo anterógrado durante la valvuloplastia aórtica con balón de perfusión.
_
Referencias Bibliográficas
1.- Grube E, Naber C, Abizaid A, Sousa E, Mendiz O, Lemos P, Kalil Filho R, Mangione J, Buellesfeld L. Feasibility of transcatheter aortic valve implantation without balloon pre-dilation: a pilot study. JACC Cardiovasc Interv. 2011;4:751–757.
2.- Wendler O, Dworakowski R, Monaghan M, MacCarthy PA. Direct transapical aortic valve implantation: a modified transcatheter approach avoiding balloon predilatation. Eur J Cardiothorac Surg. 2012;42:734–736.
3.- Eltchaninoff H, Durand E, Borz B, Furuta A, Bejar K, Canville A, Farhat A, Fraccaro C, Godin M, Tron C, Sakhuja R, Cribier A. Balloon aortic valvuloplasty in the era of transcatheter aortic valve replacement: acute and long-term outcomes. Am Heart J. 2014;167:235–240.
4.- Kumar A, Paniagua D, Hira RS, Alam M, Denktas AE, Jneid H. Balloon aortic valvuloplasty in the transcatheter aortic valve replacement era. J Invasive Cardiol. 2016;28:341–348.
5.- Campelo-Parada F, Nombela-Franco L, Urena M, Regueiro A, Jiménez-Quevedo P, Del Trigo M, Chamandi C, Rodríguez-Gabella T, Auffret V, Abdul-Jawad Altisent O, DeLarochellière R, Paradis JM, Dumont E, Philippon F, Pérez-Castellano N, Puri R, Macaya C, Rodés-Cabau J. Timing of Onset and Outcome of New Conduction Abnormalities Following Transcatheter Aortic Valve Implantation: Role of Balloon Aortic Valvuloplasty. Rev Esp Cardiol (Engl Ed). 2017 May 27.
6.- Bagur R, Kwok CS, Nombela-Franco L, Ludman PF, de Belder MA, Sponga S, Gunning M, Nolan J, Diamantouros P, Teefy PJ, Kiaii B, Chu MW, Mamas MA. Transcatheter aortic valve implantation with or without preimplantation balloon aortic valvuloplasty: a systematic review and meta-analysis. J Am Heart Assoc. 2016;5:e003191. DOI: 10.1161/JAHA.115.003191.
7.- Kuljit Singh, Kristin Carson, Onn Akbar Ali, Rohan Jayasinghe, Alexander Dick, Christopher Glover, Marino Labinaz. Efficacy and Complications of Transcatheter Aortic Valve Implantation With and Without Balloon Aortic Valvuloplasty. J Heart Valve Dis. 2017 Mar;26(2):139-145.
8.- Bonaros N, Kofler M, Frank D, Cocchieri R, Jagielak D, Aiello M, Lapeze J, Laine M, Chocron S, Muir D, Eichinger W, Thielmann M, Labrousse L, Bapat V, Rein KA, Verhoye JP, Gerosa G, Baumbach H, Deutsch C, Bramlage P, Thoenes M, Romano M. Balloon-expandable transaortic transcatheter aortic valve implantation with or without predilation. J Thorac Cardiovasc Surg. 2017 Nov 2.
9.- Fiorina C, Maffeo D, Curello S, Lipartiti F, Chizzola G, D’Aloia A, Adamo M, Mastropierro R, Gavazzi E, Ciccarese C, Chiari E, Ettori F. Direct transcatheter aortic valve implantation with self-expandable bioprosthesis: feasibility and safety. Cardiovasc Revasc Med. 2014;15:200–203.
10.- Kim WK, Praz F, Blumenstein J, Liebetrau C, Gaede L, Van Linden A, Hamm C. Walther T, Windecker S, Mollmann H. Transfemoral aortic valve implantation of Edwards SAPIEN 3 without predilatation. Catheter Cardiovasc Interv.2017;89:E38–E43.
11.- Usefulness of Echocardiographic Criteria for Transcatheter Aortic Valve Implantation without Balloon Predilation: A Single-Center Experience. Islas, Fabián et al. Journal of the American Society of Echocardiography , Volume 28 , Issue 4 , 423 – 429.
12.- Giordano A, Corcione N, Biondi-Zoccai G, Berti S, Petronio AS, Pierli C, Presbitero P, Giudice P, Sardella G, Bartorelli AL, Bonmassari R, Indolfi C, Marchese A, Brscic E, Cremonesi A, Testa L, Brambilla N, Bedogni F. Patterns and trends of transcatheter aortic valve implantation in Italy: insights from RISPEVA. J Cardiovasc Med. 2017;18:96–102



